本试题 “下列叙述正确的是[ ]A.铝制容器可盛装热的浓H2SO4B.AgI胶体在电场中自由运动C.K与水反应比Li与水反应剧烈D.红磷在过量Cl2中燃烧生成PCl3” 主要考查您对胶体
单质铝
61. 其它金属及化合物(锌、锰、钙、金等)
单质磷及其化合物
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 胶体
- 单质铝
- 61. 其它金属及化合物(锌、锰、钙、金等)
- 单质磷及其化合物
胶体:分散质粒子直径在10-9m~10-7m之间的分散系胶粒直径的大小是胶体的本质特征
胶体可分为固溶胶、液溶胶、气溶胶
①常见的液溶胶:Fe(OH)3、AgI、牛奶、豆浆、粥等
②常见的气溶胶:雾、云、烟等;
③常见的固溶胶:有色玻璃、烟水晶等胶体的性质:
丁达尔效应:
①当光束通过氢氧化铁胶体时,可以看到一条光亮的通路,这条光亮的通路是由于胶体粒子对光线散射(光波偏离原来方向而分散传播)形成的,即为丁达尔效应。
②布朗运动:粒子在不停地、无秩序的运动
③电泳:胶体粒子带有电荷,在电场的作用下,胶体粒子在分散剂里定向移动。一般来讲:金属氢氧化物,金属氧化物的胶粒吸附阳离子,胶体微粒带正电荷;非金属氧化物,金属硫化物的胶体胶粒吸附阴离子,胶体微粒带负电荷。
④胶体聚沉:向胶体中加入少量电解质溶液时,由于加入的阳离子(或阴离子)中和了胶体粒子所带的电荷,使胶体粒子聚集成为较大的颗粒,从而形成沉淀从分散剂里析出。该过程不可逆。
胶体的特性:
(1)丁达尔效应当一束光通过胶体时,胶体内会出现一条光亮的通路,这是由胶体粒子对光线散射而形成的,利用丁达尔效应可区分胶体和浊液。
(2)介稳性:胶体的稳定性介于溶液和浊液之间,在一定条件下能稳定存在,但改变条件就有可能发生聚沉。
(3)聚沉:给胶体加热、加入电解质或加入带相反电荷的胶体颗粒等均能使胶体粒子聚集成较大颗粒,从而形成沉淀从分散剂里析出。聚沉常用来解释生活常识,如长江三角洲的形成、明矾净水等。
(4)电泳现象:在电场作用下,胶体粒子在分散剂中作定向移动。电泳现象说明胶体粒子带电。电泳常用来分离提纯胶体,如工业上静电除尘。
分散系比较:
| 分散系 | 溶液 | 胶体 | 悬浊液 | 乳浊液 |
| 分散质粒子大小 | <1nm | 1~100nm | >100nm | >100nm |
| 分散质粒子结构 | 分子、离子 | 少量分子的结合体或大分子 | 大量分子聚集成的固体小颗粒 | 大量分子聚集成的液体小液滴 |
| 特点 | 均一、透明、稳定 | 多数均一、透明、较稳定 | 不均一、不透明、久置沉淀 | 不均一、不透明、久置分层 |
| 能否透过滤纸 | 能 | 能 | 不能 | —— |
| 实例 | 食盐水、蔗糖溶液 | Fe(OH)3(胶体)、淀粉胶体 | 泥水、石灰乳 | 牛奶、油漆 |
胶体发生聚沉的条件:
因胶粒带电,故在一定条件下可以发生聚沉:
- 向胶体中滴加电解质
- 向胶体中加入带相反电荷胶粒的胶体
- 加热
常见的胶体的带电情况:
- 胶粒带正电荷的胶体有:金属氧化物、金属氢氧化物。例如Fe(OH)3、Al(OH)3等。
- 胶粒带负电荷的胶体有:非金属氧化物、金属硫化物、硅酸胶体、土壤胶体。
- 胶粒不带电的胶体有:淀粉胶体。
- 特殊的,AgI胶粒随着AgNO3和KI相对量不同,而带正电或负电。若KI过量,则AgI胶粒吸附较多I-而带负电;若AgNO3过量,则因吸附较多Ag+而带正电。
注意:胶体不带电,而胶粒可以带电。
Fe(OH)3胶体的制备:
操作步骤:将烧杯中的蒸馏水加热至沸腾,向沸水中滴加5~6滴饱和FeCl3溶液,继续煮沸至呈红褐色为止。
离子方程式:Fe3++3H2O=(加热)=Fe(OH)3(胶体)+3H+
点拨:(1)淀粉溶液、蛋白质溶液虽叫做溶液,但属于胶体。
(2)胶体可以是液体,也可以是固体、气体,如烟、云、雾、有色玻璃等。
铝的主要性质:
- 物理性质:
铝是银白色,具有金属光泽的固体,硬度较小,具有良好的导电性、导热性和延展性。 - 化学性质:
活泼金属,具有较强的还原性;常温下铝在浓硫酸和浓硝酸中发生钝化;既可以与酸反应又可以与碱反应。
(1)与氧气反应: (纯氧中发出耀眼的白光)
(纯氧中发出耀眼的白光)
(2)与Cl2 、S 、N2反应: (Al2S3在溶液中完全双水解)
(Al2S3在溶液中完全双水解)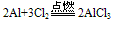
 (AlN与水反应生成Al(OH)3和NH3↑)
(AlN与水反应生成Al(OH)3和NH3↑)
(3)与水反应: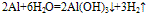
(4)与酸反应: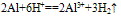
(5)与碱的反应:
(6)铝热反应:2Al+Fe2O3=(高温)=Al2O3+2Fe - 铝的用途
纯铝制作导线,铝合金用于制造飞机、汽车、生活用品等。
铝的特殊性质:
铝既能与酸反应,也能与强碱反应。
铝与酸反应:铝与浓硫酸在常温下发生钝化,2Al+6HCl==2AlCl3+3H2↑
铝与碱反应:2Al+2NaOH+2H2O==2NaAlO2+3H2↑
铝热反应:
铝热法是一种利用铝的还原性获得高熔点金属单质的方法。此种反应被称为铝热反应。
可简单认为是铝与某些金属氧化物(如Fe2O3、Fe3O4、Cr2O3、V2O5等)或非金属氧化物(如SiO2等)在高热条件下发生的反应。
铝热反应常用于冶炼高熔点的金属,并且它是一个放热反应,
其中镁条为引燃剂,氯酸钾为助燃剂。
其装置如下图所示: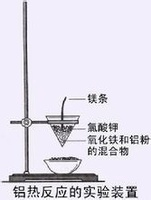
铝热反应配平技巧:
取反应物和生成物中氧化物中两边氧的最小公倍数,即可快速配平,如8Al+3Fe3O4=4Al2O3+9Fe中,可取Fe3O4和Al2O3中氧的最小公倍数12,则Fe3O4前应为3Al2O3前应为4,然后便可得到Al为8,Fe为9。
镁铝的化学性质比较:
| 单质 | 镁 | 铝 |
| 与非金属反应 | 2Mg+O2=(点燃)=2MgO (发出耀眼白光) Mg+Cl2=(点燃)=MgCl2 3Mg+N2=(点燃)=Mg3N2 |
4Al+3O2=(加热)=2Al2O3 2Al+3Cl2=(加热)=2AlCl3 2Al+3S=(加热)=Al2S3 |
| 与沸水反应 | Mg+2H2O=(加热)=Mg(OH)2+H2↑ | 不反应 |
| 与酸反应 | Mg+2H+==Mg2++H2↑ 与稀硝酸反应生成Mg(NO3)2、NOx(或者N2、NH4NO3)、H2O |
2Al+6H+==2Al3++3H2↑ 在冷的浓硝酸或浓硫酸中钝化 |
| 与氧化物反应 | 2Mg+CO2=(点燃)=2MgO+C (剧烈燃烧,生成白色粉末和黑色固体) |
2Al+Fe2O3=(高温)=2Fe+Al2O3(铝热反应) |
| 与盐溶液反应 | Mg+2NH4++2H2O==Mg2++2NH3·H2O+H2↑ Mg+Cu2+==Mg2++Cu |
2Al+3Hg2+=2Al3++3Hg |
| 与强碱反应 | 不反应 | 2Al+2OH-+2H2O==2AlO2-+3H2↑ |
铝热反应配平技巧:
取反应物和生成物中氧化物中两边氧的最小公倍数,即可快速配平,如8Al+3Fe3O4=4Al2O3+9Fe中,可取Fe3O4和Al2O3中氧的最小公倍数12,则Fe3O4前应为3Al2O3前应为4,底下便可得到Al为8,Fe为9。
铝与酸、碱反应的计算技巧:
铝与酸、碱反应的实质都是 ,
, ,所以根据得失电子守恒可知:
,所以根据得失电子守恒可知: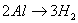 ,利用此关系可以方便地进行有关计算。
,利用此关系可以方便地进行有关计算。
铝与酸或碱溶液反应生成H2的量的计算:
Al是我们中学阶段学习的唯一既与H+反应也与OH-反应的金属,它与酸、碱反应既有相同点,也有不同点。
相同点:Al均被氧化成+3价,所以1molAl不论与H+还是与OH-反应均生成3gH2。
不同点:1molAl与H+反应消耗3molH+,而与OH-反应只消耗1molOH-,所以含有等物质的量的NaOH溶液和HCl溶液分别与足量的铝反应时生成的氢气的物质的量之比为3∶1。

“铝三角”关系:
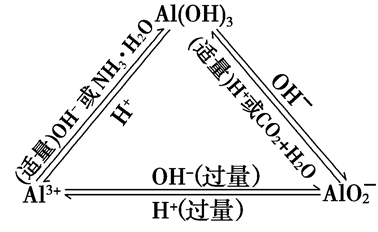
Al3++3OH-===Al(OH)3↓
Al(OH)3+OH-===AlO2-+2H2O
Al3++4OH-===AlO2-+2H2O
AlO2-+2H2O+CO2===Al(OH)3↓+HCO3-
AlO2-+H++H2O===Al(OH)3↓
AlO2-+4H+===Al3++2H2O
钝化:
铝、铁在常温下与浓硫酸发生钝化,钝化不是不反应,而是被氧化成一层致密的氧化物薄膜,恰恰说明金属的活泼性。
锌的单质及化合物:
①单质锌:
物理性质:锌化学符号是Zn,它的原子序数是30。锌是一种蓝白色金属。密度为7.14克/立方厘米,熔点为419.5℃。在室温下,性较脆;100~150℃时,变软;超过200℃后,又变脆。锌的化学性质活泼,在常温下的空气中,表面生成一层薄而致密的碱式碳酸锌膜,可阻止进一步氧化。当温度达到225℃后,锌氧化激烈。燃烧时,发出蓝绿色火焰。锌易溶于酸,也易从溶液中置换金、银、铜等。锌的氧化膜熔点高,但金属锌熔点却很低,所以在酒精灯上加热锌片,锌片熔化变软,却不落下,正是因为氧化膜的作用。锌是第四常见的金属,仅次于铁、铝及铜。
化学性质:2Zn+O2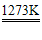 2ZnO Zn+X2
2ZnO Zn+X2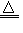 ZnX2(X=F、Cl、Br、I) 3Zn+2P
ZnX2(X=F、Cl、Br、I) 3Zn+2P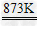 Zn3P2 Zn+S
Zn3P2 Zn+S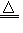 ZnS
ZnS
②氢氧化锌 Zn2++2NaOH==Zn(OH)2+2Na+ Zn(OH)2+2H+==Zn2++H2O Zn(OH)2+2OH-==[Zn(OH)4]2- Zn(OH)2+4NH3+2NH4+==[Zn(NH3)4]2++2H2O Zn(OH)2==ZnO+H2O
[Zn(NH3)4]2++2OH-==Zn(OH)2+4NH3↑
③氯化锌 ZnO+2HCl ZnCl2+H2O ZnCl2+2H2O===Zn(OH)Cl+2HCl ZnCl2+H2O=H2[ZnCl2(OH)2] FeO+H2[ZnCl2(OH)2]==Fe[ZnCl2(OH)]2+H2O Zn+CuCl2=ZnCl2+Cu
ZnCl2+H2O ZnCl2+2H2O===Zn(OH)Cl+2HCl ZnCl2+H2O=H2[ZnCl2(OH)2] FeO+H2[ZnCl2(OH)2]==Fe[ZnCl2(OH)]2+H2O Zn+CuCl2=ZnCl2+Cu
④硫化锌 2ZnO+2S==2ZnS+O2 Zn2++(NH4)2S==ZnS+2NH4+ ZnSO4+BaS==ZnS+BaSO4 Zn2++H2S==ZnS+2H+
⑤锌的配合物(a)[Zn(NH3)4]2+、(b)[Zn(CN)4]2-
钙的单质及化合物:
①单质钙:活泼金属
②氧化钙:俗称生石灰,白色块状固体;与水反应放出大量热,块状固体变成粉末状CaO+H2O==Ca(OH)2
③氢氧化钙:俗称熟石灰,常用来检验二氧化碳气体Ca(OH)2+CO2==CaCO3↓+H2O
④碳酸钙:俗称石灰石,白色固体,不溶于水,常用的建筑材料,实验室常用其和稀盐酸反应制取二氧化碳CaCO3+2HCl==CaCl2+CO2↑+H2O
银的单质及化合物:
①物理性质:银是一种化学元素,化学符号Ag,原子序数47,是一种银白色的贵金属。银性质稳定,质软富有延展性。导热,导电率高,不易受酸碱的腐蚀
②化学性质:银的特征氧化数为+1,其化学性质比铜差,常温下,甚至加热时也不与水和空气中的氧作用。但当空气中含有硫化氢时,银的表面会失去银白色的光泽,这是因为银和空气中的H2S化合成黑色Ag2S的缘故。其化学反应方程式为: 4Ag+H2S+O2=2Ag2S+2H2O
银不能与稀盐酸或稀硫酸反应放出氢气,但银能溶解在硝酸或热的浓硫酸中:2Ag+2H2SO4(浓) Ag2SO4+SO2↑+2H2O
Ag2SO4+SO2↑+2H2O
银在常温下与卤素反应很慢,在加热的条件下即可生成卤化物:
2Ag+F2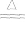 2AgF暗棕色
2AgF暗棕色
2Ag+Cl2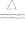 2AgCl白色
2AgCl白色
2Ag+Br2 2AgBr淡黄色
2AgBr淡黄色
2Ag+I2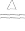 2AgI黄色
2AgI黄色
银对硫有很强的亲合势,加热时可以与硫直接化合成Ag2S:2Ag+S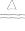 Ag2S
Ag2S
银易溶于硝酸和热的浓硫酸,微溶于热的稀硫酸而不溶于冷的稀硫酸。盐酸和王水只能使银表面发生氯化,而生成氯化银薄膜。
银具有很好的耐碱性能,不与碱金属氢氧化物和碱金属碳酸盐发生作用。
磷在自然界中的存在:
自然界中没有游离态的磷,磷主要以磷酸盐的形式存在于矿石中。磷和氮一样,是构成蛋白质的成分之一。动物的骨骼、牙齿和神经组织,植物的果实和幼芽,生物的细胞里都含有磷,磷对维持生物体正常的生理机能起着重要的作用。
磷的物理性质:
磷的单质有多种同素异形体,其中常见的是白磷和红磷。白磷和红磷的主要性质如下表。 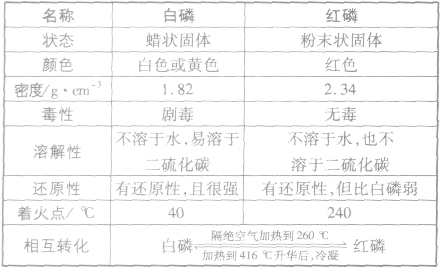
特别提醒白磷遇光会逐渐变为黄色。因此,白磷又称黄磷,白磷的颜色往往表述为“白色或黄色”。
白磷和红磷的化学性质:
白磷和红磷都能在空气或氧气中燃烧,燃烧产物一般是五氧化二磷,且反应放出大量的热,4P+5O2 2P2O5
2P2O5
磷的用途:
白磷和红磷有许多用途,如都可用于制造纯度较高的磷酸;白磷可用于制造燃烧弹、烟幕弹等;红磷可用于制农药、安全火柴等。
白磷和红磷的分子结构:
白磷的分子组成为P4,分子的空间构型为正四面体(如图A)。红磷的结构较复杂,有人认为红磷是P4分子断裂一个键后相互结合形成的长链状分子(如图B).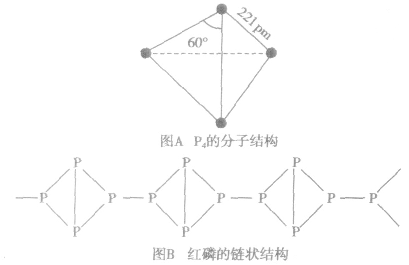
特别提醒白磷和红磷的化学式通常都写为P。
磷的化合物:
(1)五氧化二磷:
五氧化二磷的分子式为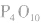 ,通常写为
,通常写为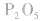 ,
,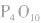 分子的空间构型如图所示。
分子的空间构型如图所示。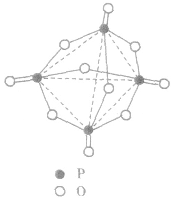
五氧化二磷通常为白色固体,由磷在空气中燃烧生成, 632K时升华。
五氧化二磷是典型的酸性氧化物,具有酸性氧化物的通性。
五氧化二磷很易跟水反应,跟冷水反应生成偏磷酸,跟热水反应生成磷酸,反应放出大量的热。 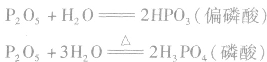
五氧化二磷的强亲水性决定了它可用作干燥剂。五氧化二磷是一种固态、酸性、无强氧化性的干燥剂,干燥能力非常强。
(2)磷酸:
磷酸为三元中强酸,属于弱电解质,易溶于水,在水中分三级电离。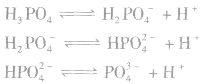
纯磷酸是无色晶体,熔点为315K.沸点较高,可溶于水。
磷酸无强氧化性,具有酸的通性。为了避免Br-、 I-被氧化,可用浓磷酸代替浓硫酸在实验室中制备HBr和HI。
(3)磷酸盐:
磷酸是三元酸,对应的盐有正盐和酸式盐: 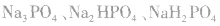 .
.
与“下列叙述正确的是[ ]A.铝制容器可盛装热的浓H2SO4B.AgI胶体...”考查相似的试题有:
- (1)在Fe(OH)3胶体中,逐滴加入HI稀溶液,会出现一系列变化。先出现红褐色沉淀,原因是______________________;(2)随后沉淀溶...
- 溶液、胶体、浊液三种分散系最本质的区别是( )A.稳定性B.透明度C.分散质微粒大小D.能否发生丁达尔现象
- 下列实验能达到目的的是A.只滴加氨水鉴别NaCl、AlCl3、MgCl2、Na2SO4四种溶液B.将NH4Cl溶液蒸干制备NH4Cl固体C.用萃取分液...
- 化学是一门以实验为基础的科学,掌握基本的实验方法和操作技能是做好化学实验的基础,下列有关化学实验基本知识的描述不正确...
- 氢氧化铁胶体逐滴加入下列溶液,先产生沉淀后沉淀溶解的是()A.稀硫酸B.酒精C.饱和硫酸钠溶液D.氯化钠溶液
- 有一包粉末状的混合物,可能含有MgCl2、FeCl3、NaOH、CuSO4、Al2(SO4)3、KNO3、CaCO3、NaCl中的两种或多种。将混合物置于水中...
- 2005年1月,美国科学家在《Science》上发表论文,宣布发现Al的超原子结构 ,如Al13、Al14。Al13、Al14的一些性质像其它的主族...
- 把4.6 g钠放入200 mL 0.1 mol·L-1AlCl3溶液中,待其充分反应后,下列叙述中错误的是( )A.Cl-的浓度几乎不变B.溶液变浑浊C...
- 某化学兴趣小组用只含有铝、铁、铜的工业废料制取纯净的氯化铝溶液、绿矾晶体(FeSO4·7H2O)和胆矾晶体,以探索工业废料的再利...
- 红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g)。反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据)。根据上图...