本试题 “氨和联氨是氮的两种常见化合物。在科学技术和生产中有重要的应用。 根据题意完成下列计算:(1)联氨用亚硝酸氧化生成氮的另一种氢化物,该氢化物的相对分子质量...” 主要考查您对金属、非金属的有关计算
有机化学的有关计算
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 金属、非金属的有关计算
- 有机化学的有关计算
包括金属及化合物、金属与非金属化合物、非金属化合物之间的反应的计算,解此类题的关键是正确的写出反应方程式,明确物质间的等量关系。明确物质之间的反应,正确写出方程式,此类题可迎刃而解。
AlCl3与NaOH反应的相关计算:
1、求Al(OH)3沉淀的量
2、求反应物碱的量
铝与酸、碱反应的计算规律:
铝分别与盐酸、氢氧化钠溶液反应的原理: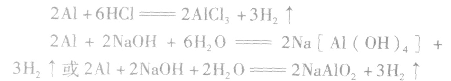
(1)等量铝分别与足量盐酸和氢氧化钠溶液反应,产生氢气的体积比为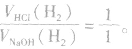
(2)足量的锅分别与等物质的量的盐酸和氢氧化钠溶液反应,产生氢气的体积比为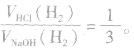
(3)一定量的铝分别和一定量的盐酸和氢氧化钠溶液反应,若产生氢气的体积比为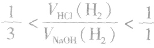 ,则必定是:
,则必定是:
①铝与盐酸反应时,铝过量而盐酸不足;
②铝与氢氧化钠溶液反应时,铝不足而氢氧化钠过量。
解有关硝酸与金属反应的计算题的技巧:
1.灵活运用得失电子守恒、原子守恒及溶液中的电荷守恒关系例如Cu与HNO3反应中就有以下等量关系:
(1)N原子守恒:反应前所有的N只存在于HNO3中;反应后含N的物质有HNO3的还原产物(假设此处有NO3、NO)和Cu(NO3)3,若HNO3过量,则过量HNO3中也含一部分N,则有:n(N)=n(NO2)+ n(NO)+2n[Cu(NO3)3]+n剩(HNO3)。
(2)得失电子守恒:在反应中失去电子的是参加反应的Cu, ;得到电子的是被还原的HNO3(假设还原产物为NO2、NO),NO3-+e→ NO2、NO3-+3e→NO。根据得失电子守恒,则有:
;得到电子的是被还原的HNO3(假设还原产物为NO2、NO),NO3-+e→ NO2、NO3-+3e→NO。根据得失电子守恒,则有: 
(3)溶液中的电荷守恒:在任何溶液中,阴离子所带负电荷总数与阳离子所带正电荷总数在数值上是相等的。在Cu与HNO3反应后的溶液中,若HNO3不过量,阳离子只有Cu2+,阴离子只有NO3-(此类计算不考虑H2O电离出的极少量的H+、OH-);若HNO3过量,溶液中阳离子有Cu2+和H+,阴离子只有NO3-。则有:
①若HNO3不过量: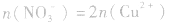
②若HNO3过量: 
2.铁与稀HNO3的反应规律 

(2)上述反应可以认为先发生反应①,若Fe有剩余则发生 ①×2+ ③即得反应②,所以,无论是反应①还是反应②,被还原的HNO3皆占参加反应的HNO3的
①×2+ ③即得反应②,所以,无论是反应①还是反应②,被还原的HNO3皆占参加反应的HNO3的 。
。
有关镁、铝的图像集锦:
Al(OH)3与Al3+、AlO2-之间的转化,是建立在 Al(OH)3两性基础上的,有关相互转化的配比和沉淀Al(OH)3的质量变化,见下表:
包括确定有机物分子中元素质量比,所含原子个数,有机物燃气确定其组成,确定有机物分子中元素质量分数,确定有机物分子式、结构简式等。确定有机物分子式、结构简式的计算: (1)先求有机物的最简式和相对分子质量,再依(最简式相对分子质量)n=相对分子质量,求得分子式,再根据题中给的信息确定有机物的官能团,进而确定有机物的结构简式。
(2)商余法适用于烃分子式的确定:商为C原子数,余数为H原子数。注意:一个C原子的质量=12个H原子的质量
有机物分子式的确定:
1.有机物组成元素的判断一般来说,有机物完全燃烧后各元素对应的产物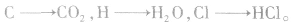 若某有机物完全燃烧后产物只有
若某有机物完全燃烧后产物只有 则其组成元素可能为 C、H或C、H、O。欲判断该有机物是否含氧元素,首先应求出产物CO2中碳元素的质量及H2O中氢元素的质量,然后将C、H的质量之和与原来有机物的质量比较,若二者相等,则原有机物中不含氧元素;若有机物的质量大于C、H的质量之和,则原有机物中含氧元素。
则其组成元素可能为 C、H或C、H、O。欲判断该有机物是否含氧元素,首先应求出产物CO2中碳元素的质量及H2O中氢元素的质量,然后将C、H的质量之和与原来有机物的质量比较,若二者相等,则原有机物中不含氧元素;若有机物的质量大于C、H的质量之和,则原有机物中含氧元素。
2.确定有机物分子式的方法
(1)实验式法:实验式又叫最简式。
(2)物质的量关系法:由密度或其他条件 求摩尔质量
求摩尔质量 求1moL分子中所含元素原子的物质的量
求1moL分子中所含元素原子的物质的量 求分子式。
求分子式。
(3)化学方程式法(代数法):利用化学方程式 列方程组
列方程组 求解未知数值
求解未知数值 求分子式。
求分子式。
(4)通式法:题干要求或物质性质 类别及组成通式
类别及组成通式 n值
n值 分子式。
分子式。
3.相对分子质量的测定方法
相对分子质量的测定方法——质谱法,找最大质荷比,确定相对分子质量。
4.有机物的相对分子质量的相关规律
(1)设烃的混合物的平均相对分子质量为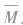 ,平均分子式为
,平均分子式为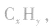 则:
则:
①若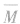 <26,则一定有CH4;
<26,则一定有CH4;
②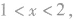 则一定有CH4;
则一定有CH4;
③若y<4,则一定有C2H2。
(2)最简式相同规律
①含有n个碳原子的饱和一元醛与含有2n个碳原子的饱和一元羧酸和饱和一元酯具有相同的最简式 (n≥2)。
②含有n个碳原子的炔烃与含有3n个碳原子的苯及其同系物具有相同的最简式。最简式相同的有机物,无论多少种,以何种比例混合,混合物中元素质量比例相同。
(3)相对分子质量相同规律
①同分异构体的相对分子质量必然相同。
②含有n个碳原子的一元醇与含(n—1)个碳原子的同类型一元羧酸和一元酯的相对分子质量相同。
③含有n个碳原子的烷烃与(n—1)个碳原子的饱和一元醛,即 的相对分子质量相同。
的相对分子质量相同。
④常见的相对分子质量相同的有机物和无机物有:
a.相对分子质量为28的有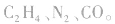
b.相对分子质量为30的有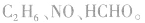
c.相对分子质量为44的有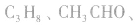

d.相对分子质量为46的有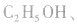
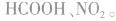
e.相对分子质量为60的有
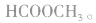
(4)由相对分子质量求烃的分子式
设烃的相对分子质量为M,由 可知:
可知:
若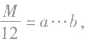 则烃的分子式为
则烃的分子式为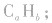 若b为0,则烃的分子式为
若b为0,则烃的分子式为 若b太小而不合理,则可变换为
若b太小而不合理,则可变换为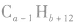 (减碳增氢法,减1个C原子,增加12个H原子)。如
(减碳增氢法,减1个C原子,增加12个H原子)。如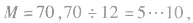 分子式为
分子式为 又如
又如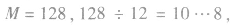 分子式为
分子式为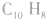 (萘)或
(萘)或 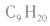 (壬烷)。
(壬烷)。
酚类化合物与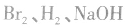 反应时最大用量的计算:
反应时最大用量的计算:
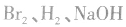 溶液是有机反应中的常见试剂,它们能参与的反应有哪些呢?
溶液是有机反应中的常见试剂,它们能参与的反应有哪些呢?
1.Br2:①与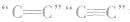 等发生加成反应;
等发生加成反应;
②取代酚羟基邻位、对位上的氢原子;
③取代饱和碳原子上的氢原子。
2.H2:与有机物中的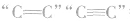 ,
,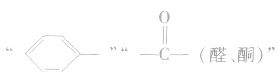 等发生加成反应。
等发生加成反应。
3.NaOH溶液:与酚、羧酸发生中和反应(但不与醇反应),催化卤代烃、酯等的水解并与水解生成的氢卤酸、酚、羧酸等发生中和反应。
注意:
①发生加成反应时,断裂双键或三键中的1mol键消耗1molBr2或H2;发生取代反应时,1molBr2只取代1mol(而不是2mol)氢原子(同时生成1molHBr)。
②H2不与羧酸、酯基及羧酸酐中的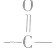 发生加成反应.
发生加成反应.
与“氨和联氨是氮的两种常见化合物。在科学技术和生产中有重要的...”考查相似的试题有:
- 两份铝屑,第一份与足量的稀盐酸反应,第二份与足量的氢氧化钠溶液反应,产生氢气的体积比为1:2(同温同压下),则两份铝屑的...
- 在铁与铜的混合物中,加入一定量的稀HNO3,充分反应后剩余m1g 金属,再向其中加入一定量的稀H2SO4,充分振荡后,剩余m2g 金属...
- 某学生用NaHCO3和KHCO3组成的某混合物进行实验,现称取不同质量的混合物溶于水后,分别滴入相同浓度的盐酸50 mL,产生CO2气体...
- 某有机化合物A的相对分子质量大于100,小于130。经分析得知,其中碳和氢的质量分数之和为46.66%,其余为氧,则该化合物分子中...
- 1mol 某芳香烃完全燃烧得到8 mol的CO2和5 mol 的H2O ,请回答下列问题:(1)该芳香烃的分子式为________。(2)若该烃只有一...
- 在某温度下,反应H2(g)+CO2(g)H2O(g)+CO(g) △H>0的平衡常数K=2. 25。该温度下在甲、乙、丙三个恒容(体积均为2 L)密闭容器中...
- TMB是一种应用指纹检测新型安全的色原试剂.已知TMB中含有碳、氢、氮三种元素,其相对分子质量为240.为测定TMB的组成,用下...
- 2004年诺贝尔化学奖授予阿龙·切哈诺沃等三位科学家,以表彰他们发现了泛素调节的蛋白质降解。化合 物A是天然蛋白质水解的最终...
- 写出符合下列要求的有机物的结构简式:(1)燃烧后生成CO2和H2O的物质的量之比为2的两种常见的烃:_________,_________;一...
- 一定温度下,W g下列物质在足量氧气中充分燃烧,产物与过量的Na2O2完全反应,Na2O2固体增重W g,符合此要求的组合是( )①H2 ②C...