本试题 “某种酶是由419个氨基酸形成的蛋白质。科学家利用生物技术做出5种不同长度的该酶的片段,并分别测定其活性如下图所示,分析该酶可能具有活性的是[ ]A.第1号氨...” 主要考查您对蛋白质的结构
酶的本质与特性
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 蛋白质的结构
- 酶的本质与特性
1、蛋白质的结构层次:

2、蛋白质种类多样性的原因:
(1)氨基酸的原因:
①氨基酸的种类不同。
②氨基酸的数目成百上千。
③氨基酸的排列顺序千变万化。
(2)肽链的原因:
肽链的盘曲、折叠方式及其形成的空间结构千差万别。
知识点拨:
1、脱去的水分子中的氢来自氨基和羧基,氧来自羧基。
2、肽键的写法有以下几种,这三种都是正确的。
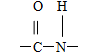 或-CO-NH-或-NH-CO-
或-CO-NH-或-NH-CO- 3、多肽中具体有几个氨基或几个羧基,应关注R基中是否有氨基或羧基。
4、若形成的多肽链是环状:氨基酸数=肽键数=失去水分子数。
5、在蛋白质分子量的计算中若通过图示或其他形式告知蛋白质分子中含有二硫键时,要考虑脱去氢的质量,每形成一个二硫键,脱去2个H。
知识拓展:
氨基酸形成多肽过程中的相关计算
1、蛋白质分子量、氨基酸数、肽链数、肽键数和脱去水分子数的关系
(1)肽键数=脱去水分子数=氨基酸数一肽链数;
(2)蛋白质分子量=氨基酸数目x氨基酸平均相对分子质量一脱去水分子数×18。
| 肽链数目 | 酸数氨基 | 脱去水分子数 | 多肽链分子量 | 氨基数目 | 羧基数目 | |
| 1条 | m | m-1 | m-1 | am-18(m-1) | 至少1个 | 至少1个 |
| 2条 | m | m-n | m-n | am-18(m-n) | 至少n个 | 至少1个 |
2、蛋白质中游离氨基或羧基数的计算
(1)至少含有的游离氨基或羧基数=肽链数
(2)游离氨基或羧基数=肽链数+R基中含有的氨基或羧基数
3、蛋白质中含有N、O原子数的计算 (1)N原子数=肽键数+肽链数+R基上的N原子数=各氨基酸中N原子总数。
(2)O原子数=肽键数+2×肽链数+R基上的O原子数=各氨基酸中O原子总数一脱去水分子数。
4、巧记氨基酸结构通式让学生把自己身体想象成一个氨基酸分子:中央C原子、头-H原子、右手——氨基(-NH2)左手——羧基(-COOH)、脚-R基(-R)
5、巧记脱水缩合过程 首先由两个人手拉手,一个人出左手拉住另一个人的右手,脱去一分子水,形成二肽。然后再加上一个人,又脱去一分子水,形成三肽,以此类推,形成多肽。
1.酶的作用:降低活化能。
(1)活化能:分子从常态转变为容易发生化学反应的活跃状态所需要的能量。
(2)作用机理:酶能降低化学反应所需的活化能,使一个原本在较温和条件下不能进行的反应可以高效快速地进行。
2.酶的本质及实验验证
(1)酶本质的探索
| 时间 | 发现者 | 实验过程及现象 | 实验结论 |
| 1773年 | 意大利科学家斯帕兰札尼 | 将装有肉块的小金属笼子让鹰吞下,一段时间后取出,发现笼内的肉块不见了 | 说明胃具有化学性消化的作用 |
| 1836年 | 德国科学家施旺 | 从胃液中提取出了消化蛋白质的物质 | 这就是胃蛋白酶 |
| 1926年 | 美国科学家萨姆纳 | 从刀豆种子中提取出脲酶的结晶,并进行了证明脲酶是蛋白质的化学实验 | 证明脲酶是一种蛋白质 |
| 20世纪30年代 | 许多科学家 | 提取多种酶的蛋白质结晶 | 酶是一类具有生物催化作用的蛋白质 |
| 20世纪 80年代 | 美国科学家切赫和奥特曼 | 少数RNA也具有生物催化功能 | 少数的酶是RNA |
(2)酶的本质
| 化学本质 | 绝大多数是蛋白质 | 少数是RNA |
| 合成原料 | 氨基酸 | 核糖核苷酸 |
| 合成场所 | 核糖体 | 细胞核(真核生物)(主要) |
| 来源 | 一般来说,活细胞都能产生酶 | |
(3)酶化学本质的实验验证
①证明某种酶是蛋白质
实验组:待测酶液+双缩脲试剂一—是否出现紫色反应。
对照组:标准蛋白质溶液+双缩脲试剂——出现紫色反应。
②证明某种酶是RNA
实验组:待测酶液+吡罗红染液——是否呈现红色。
对照组:标准RNA溶液+吡罗红染液——出现红色。
酶的特性及应用:
1、酶的特性
(1)高效性:酶的催化效率是无机催化剂的107~ 103倍,这说明酶具有高效性的特点。
(2)专一性:每一种酶只能催化一种化合物或一类化合物的化学反应,这说明酶的催化作用具有专一性的特点,酶的专一性的解释常用“锁和钥匙学说”。
(3)温和性:绝高温都能使蛋白质其他化学键的断裂永久失活。但低温酶活性可以恢复。
2、酶的特性在生产生活中的应用
(1)人在发烧时,不想吃东西,其原因是温度过高导致消化酶的活性降低。
(2)唾液淀粉酶随食物进入胃内,不能继续将淀粉分解为麦芽糖。原因是唾液淀粉酶的最适pH在7左
(3)胰岛素制剂是治疗糖尿病的有效药物,只能注射,不能口服,其原因是胰岛素是一种蛋白质,若口服会被蛋白酶水解。
1、酶的作用和特性的实验探究:
1.酶的催化作用实验探究对照组:反应物+清水检测反应物不被分解;实验组:反应物+等量的相应酶溶液检测反应物被分解。
2.酶的专一性实验搽究此实验中的自变量可以是不同反应物,也可以是不同酶溶液,因变量是反应物是否被分解。
(1)设计思路一:换反应物不换酶
实验组:反应物+相应酶溶液检测反应物被分解;
对照组:另一反应物+等量相同酶溶液检测反应物不被分解。
(2)设计思路二:换酶不换反应物
实验组:反应物+相应酶溶液检测反应物被分解;
对照组:相同反应物+等量另一种酶溶液检测反应物不被分解。
3.酶的高效性实验探究
对照组:反应物+无机催化剂检测底物分解速率;
实验组:反应物+等量酶溶液检测底物分解速率。
实验中自变量是无机催化剂和酶,因变量是底物分解速率。
4.酶作用的适宜条件的探究
(1)最适温度的探究实验原理
①淀粉+淀粉酶——麦芽糖;麦芽糖+斐林试剂—一产生砖红色沉淀;淀粉+碘——蓝色。
②温度影响淀粉酶活性,从而影响淀粉的分解,滴加碘液后,根据蓝色深浅来判断淀粉分解状况,进而推断出酶活性变化。
(2)最适pH的探究实验原理
①2H202+过氧化氢酶——2H2O+O2
②pH影响酶的活性,从而影响氧气的生成速度,可用点燃但无火焰的卫生香燃烧的情况来检验氧气生成速度的快慢。
(3)实验探究思路
①最适温度的探究思路 
②最适pH的探究思路
2、易错点拨:
(1)在酶的最适pH探究实验中,操作时必须先将酶置于不同环境条件下(加清水、加氢氧化钠、加盐酸),然后再加入反应物。不能把酶加入反应物在酶的作用下先发生水解。
(2)在酶的最适温度探究实验中,酶溶液和反应物混合之前,需要把两者先分别放在各自所需温度下保温一段时间。若选择淀粉和淀粉酶来探究酶的最适温度,检测的试剂宜先用碘液,不应该选用斐林试剂。因选用斐林试剂需热水浴加热,而该实验中需严格控制温度。
知识拓展:
1、利用酶的专一性也可探究某种酶的化学本质是蛋白质还是RNA:将某种酶用蛋白酶或核糖核酸酶处理,根据处理后的酶液是否还有催化作用予以判断。
2、一般情况下,加热也能加快化学反应速率,其作用机理是直接供能,使底物分子从常态转变为易发生反应的活跃状态,其过程并不改变活化能的大小。
3、人体消化道各段消化酶的最适pH:
口腔:唾液淀粉酶,最适pH为6.8(中性);
胃:胃蛋白酶,最适pH为1.5-2.2(酸性);
小肠:肠液、胰液中的各种酶,最适pH为8.0~9.0(弱碱性)。
胃液的pH在2左右,唾液淀粉酶在胃中会使失活并以蛋白质的形式被胃蛋白酶水解
4、植物体内的酶最适pH大多在4.5-6.5之间。
例 下列有关酶的反应与作用叙述,正确的是 ( )
A.酶具有催化作用是因为酶可以提高反应的活化能
B.酶的合成原料是氨基酸或脱氧核苷酸
C.所有的酶都在核糖体上合成
D.所有的酶都是有机物
答案D
5、具有专一性的物质归纳
(1)酶:每一种酶只能催化一种或一类化学反应。如限制性核酸内切酶能识别特定的核苷酸序列,并在特定的切点上切割DNA分子。
(2)载体:某些物质通过细胞膜时需要载体协助,不同物质所需载体不同,载体的专一性是细胞膜选择透过性的基础。
(3)激素:激素特异性地作用于靶细胞、靶器官,其原因在于它的靶细胞膜或胞内存在与该激素特异性结合的受体。
(4)tRNA:tRNA有61种,每种tRNA只能识别并转运一种氨基酸。
(5)抗体:一种抗体只能与相应的抗原发生特异性结合。
与“某种酶是由419个氨基酸形成的蛋白质。科学家利用生物技术做出...”考查相似的试题有:
- 淀粉、唾液淀粉酶和控制合成唾液淀粉酶的DNA,它们的基本组成单位依次是[ ]A.葡萄糖、葡萄糖和氨基酸B.葡萄糖、氨基酸和脱...
- 某蛋白质由A、B、两条肽链构成,A链含有21个氨基酸,B链含有30个氨基酸,缩合时形成的水分子数为:[ ]A.48B.49C.50D.51
- 含有215个N原子的200个氨基酸,形成了5个四肽、4个六肽和一个2条肽链构成的蛋白质分子。这些多肽和蛋白质分子中,肽键与氨基...
- 图甲是H2O2酶活性受pH影响的曲线,图乙表示在最适温度下,pH=b时H2O2分解产生的O2量随时间的变化。若该酶促反应过程中改变某...
- 某种蛋白酶是由129个氨基酸脱水缩合形成的蛋白质,下列叙述正确的是[ ]A.该蛋白酶分子结构中至少含有129个氨基和129个羧基B...
- 用纯唾液和用稀释10倍的唾液做唾液淀粉酶的催化实验,其效果完全相同,这说明酶具有[ ]A.催化性B.专一性C.高效性D.稳定性
- 将1mL5%的新鲜唾液倒入装有10mL糨糊的试管内,置于25℃的温水中水浴加热,下列各方法中能提高试管内反应速率的是[ ]A.向试管...
- 下图表示某有机物加入某种酶后在0~80℃环境中,有机物的分解总量与温度的关系图。据图判断,在0~80℃环境中,酶的活性变化曲...
- 下列有关酶的叙述不正确的是[ ]A.酶比无机催化剂更能显著降低化学反应活化能B.淀粉酶被水解的最终产物是氨基酸C.光合作用...
- 关于酶的叙述中,不正确的是[ ]A.酶在细胞外也能起作用B.酶能降低化学反应的活化能C.绝大多数的酶是在核糖体上合成的D.酶...