本试题 “Na2CO3和H2O2结合成棒状晶体,Na2CO3·xH2O2(过氧化氢合相当于水合。注意:使用高浓度H2O2时一定要小心,防止爆炸生成水和氧气),可消毒、漂白或作O2源…。现...” 主要考查您对碳酸钠
过氧化氢
等电子原理(等电子体)
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 碳酸钠
- 过氧化氢
- 等电子原理(等电子体)
碳酸钠(Na2CO3):
(1)俗名:纯碱或苏打;白色粉末,易溶于水,稳定;可用于制玻璃、肥皂、造纸、防治等
(2)与H+反应:CO32-+2H+==CO2↑+H2O
(3)与NaOH不反应
(4)与石灰水反应:CO32-+Ca2+==CaCO3↓
(5)与氯化钡反应:CO32-+Ba2+==BaCO3↓
(6)与CO2反应:CO32-+CO2+H2O==2HCO3-
碳酸钠的物理性质:
碳酸钠常温下为白色粉末或颗粒。溶于水和甘油,不溶于乙醇。水溶液呈强碱性,pH11.6。
碳酸钠是一种强碱盐,溶于水后发生水解反应(碳酸钠水解会产生碳酸氢钠和氢氧化钠),使溶液显碱性,有一定的腐蚀性,能与酸进行复分解反应。
稳定性 稳定性较强,但高温下也可分解,生成氧化钠和二氧化碳。长期暴露在空气中能吸收空气中的水分及二氧化碳,生成碳酸氢钠,并结成硬块。吸湿性很强,很容易结成硬块,在高温下也不分解。含有结晶水的碳酸钠有3种:Na2CO3·H2O、Na2CO3·7H2O和Na2CO3·10H2O。
碳酸钠的用途:
用于制玻璃、肥皂、造纸、纺织等工业,也用作食品工业发酵剂。
Na2CO3、NaHCO3的性质比较:
| 表示 | 名称 | 碳酸钠 | 碳酸氢钠 |
| 化学式 | Na2CO3 | NaHCO3 | |
| 俗称 | 苏打 | 小苏打 | |
| 物理性质 | 色态 | 白色粉末 | 白色晶体 |
| 溶解性 | 易溶于水 | 能溶于水 | |
| 化学性质 | 与盐酸反应 | Na2CO3+2HCl=2NaCl+H2O+CO2↑ | NaHCO3+HCl=NaCl+H2O+CO2↑ |
| 热稳定性 | 很稳定 | 受热分解:2NaHCO3=(加热)=Na2CO3+H2O+CO2↑ | |
| 与NaOH反应 | 不反应 | NaHCO3+NaOH=Na2CO3+H2O | |
| 相互转化 | Na2CO3+H2O+CO2=2NaHCO3 | NaHCO3+NaOH=Na2CO3+H2O 2NaHCO3=(加热)=Na2CO3+H2O+CO2↑ |
Na2CO3、NaHCO3的鉴别:

Na2CO3、NaHCO3与足量盐酸反应的比较:
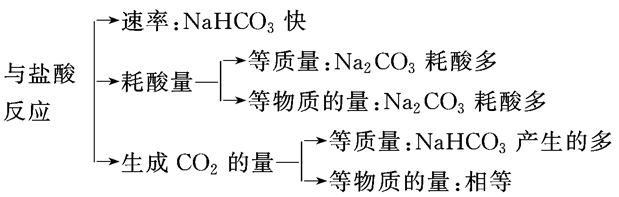
Na2CO3溶液与盐酸反应:
滴加顺序不同,现象不同,化学方程式不同。
①向盐酸里逐滴加入Na2CO3溶液(开始时酸过量) 2HCl+Na2CO3===2NaCl+CO2↑+H2O
②向Na2CO3溶液里逐滴加入盐酸(开始时酸不足) HCl+Na2CO3==NaCl+NaHCO3(无气泡) HCl+NaHCO3==NaCl+CO2↑+H2O(后来有气泡)
[特别提醒]
(1)Na2CO3和盐酸可以用互滴法鉴别。
(2)滴加顺序不同,放出CO2的量可能相同,也可能不同。
碳酸钠、碳酸氢钠与盐酸反应的基本图像的归纳总结:
(1)向Na2CO3中逐滴加入盐酸,消耗HCl的体积与产生CO2的体积的关系如图1所示;
(2)向NaHCO3中逐滴加入盐酸,消耗HCl的体积与产生CO2的体积的关系如图2所示;
(3)向NaOH、Na2CO3的混合物中逐滴加入盐酸,消耗HCl的体积与产生CO2的体积的关系如图3所示(设NaOH、Na2CO3的物质的量之比x∶y=1∶1,其他比例时的图像略);
(4)向Na2CO3、NaHCO3的混合物中逐滴加入盐酸,消耗HCl的体积与产生CO2的体积的关系如图4所示(设Na2CO3、NaHCO3的物质的量之比m∶n=1∶1,其他比例时的图像略)。
过氧化氢:
俗称,双氧水,基本结构为H-O-O-H,但并不是直线结构,因此有极性,是极性分子;O上有孤电子对,因此O-O键很弱易断。
过氧化氢和水的性质比较:


等电子原理:
1.等电子原理等电子体具有相似的化学键特征,它们的结构相似,物理性质相近,此原理称为等电子原理。例如,CO和N2的熔沸点、溶解性、分子解离能等都非常相近。
2.等电子粒子电子数相同的粒子(原子、分子、离子)称为等电子粒子。
常见的等电子粒子: 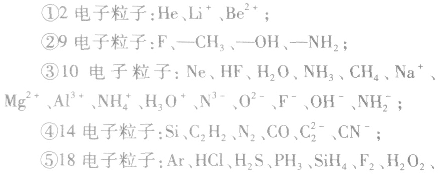
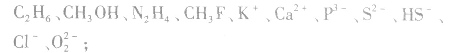
⑥核外电子总数及质子数均相等的粒子: 
3.等电子体
(1)原子总数相同、价电子总数相同的粒子互称为等电子体。如N2与CO是等电子体,但N2与C2H2不是等电子体;O2与SO2是等电子体。
(2)常见的等电子体
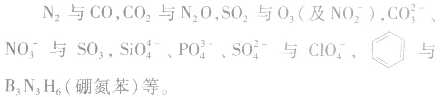
4.等电子原理的应用
(1)利用等电子原理可以较快判断一些分子或离子的构型,如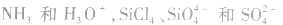 的空间构型分别是三角锥形和正四面体形。
的空间构型分别是三角锥形和正四面体形。
(2)在制造新材料方面有重要应用。如晶体硅、锗是良好的半导体材料,它们的等电子体磷化铝(AIP)、砷化镓(GaAs)也都是良好的半导体材料。,
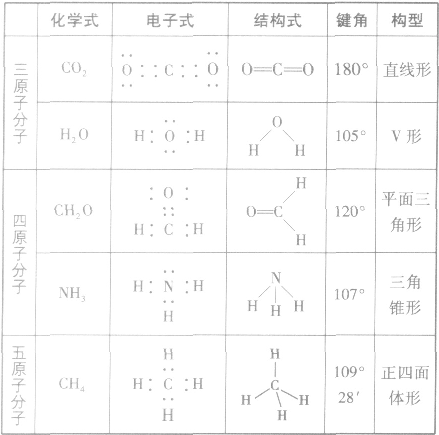
常见分子的立体结构:
与“Na2CO3和H2O2结合成棒状晶体,Na2CO3·xH2O2(过氧化氢合相当...”考查相似的试题有:
- 25℃时,浓度均为0.2 mol·L-1的NaHCO3和Na2CO3溶液中,下列判断正确的是[ ]A.后者仅存在着水解平衡,不存在着电离平衡B.两溶液...
- 某研究性学习小组将一定浓度的Na2CO3溶液滴入CuSO4溶液中得到蓝色沉淀。甲同学认为两者反应只生成CuCO3一种沉淀;乙同学认为...
- 实验室有甲、乙两瓶丢失标签的无色溶液,其中一瓶是盐酸,另一瓶是Na2CO3溶液,为确定甲、乙的成分及其物质的量浓度,现操作...
- X、Y、Z、W四种化合物均由短周期元素组成,其中X含有四种元素,X、Y、Z的焰色反应均为黄色,W为无色无味气体。这四种化合物具...
- 我国著名的化工专家侯德榜在20世纪20年代所创立的“侯氏制碱法”誉满全球。“侯氏制碱法”中的碱是指下列的[ ]A.NaOHB.K2CO3C....
- A、B、C、D、E五种物质都含1~18号元素中的某一元素,它们按下图所示关系相互转化,已知A为金属单质。写出A~E的化学式:A.__...
- 已知X 、Y、 Z 、W、 N是短周期中原子序数依次增大的五种主簇元素,通常情况下Y形成的单质为固体,其余的为气体。N是第三周期...
- 由Fe2O3、Fe、CuO、C、Al中的几种物质组成的混合粉末,取样品进行下列实验(部分产物略去)(1)取少量溶液X,加入过量的NaOH溶液...
- 为保证鱼苗长距离顺利运输,必须满足三个条件:①保持适量的氧气;②及时排出鱼苗呼出的二氧化碳;③水溶液应显弱碱性,防止细菌...
- 氮可以形成多种离子,如N3-,NH2-,N3-,NH4+,N2H5+,N2H62+等,已知N2H5+与N2H62+是由中性分子结合质子形成的,类似于NH4+...