本试题 “已知X+、Y3+、Z-、W2-是短周期元素X、Y、Z、W形成的离子,甲、乙、丙均是由上述四种离子中的两种组成的化合物。甲、乙、丙溶于水所得溶液分别呈酸性、碱性和...” 主要考查您对氧化钠
其他钠盐(氯化钠、硫化钠、氮化钠等)
铝盐(铝离子)
元素的推断
原电池电极反应式的书写
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 氧化钠
- 其他钠盐(氯化钠、硫化钠、氮化钠等)
- 铝盐(铝离子)
- 元素的推断
- 原电池电极反应式的书写
氧化钠的基本性质:
白色固体,碱性氧化物,不稳定
(1)与水反应:Na2O+H2O==2NaOH
(2)与CO2反应:Na2O+CO2==Na2CO3
(3)与HCl反应:Na2O+2HCl==2NaCl+H2O
氧化钠与过氧化钠的比较:
| 物质 | 氧化钠 | 过氧化钠 |
| 色态 | 白色固体 | 淡黄色固体 |
| 类别 | 碱性氧化物 |
过氧化物(不属于碱性氧化物) |
| 化学键类型 | 仅含离子键 | 离子键和非极性键 |
| 电子式 | 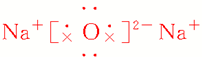 |
 |
| 生成条件 | 常温 | 点燃或加热 |
| 氧的化合价 | -2 | -1 |
| 阴阳离子个数比 | 1:2 | 1:2 |
| 稳定性 | 不稳定 | 稳定 |
| 转化关系 | 2Na2O+O2=2Na2O2 | |
| 用途 | 用于制取少量过氧化钠 | 供氧剂、漂白剂、氧化剂 |
| 与水反应方程式 | 2Na2O+2H2O=2NaOH | 2Na2O2+2H2O=4NaOH+O2↑ |
| 与CO2反应 | Na2O+CO2=NaCO3 | 2Na2O2+2CO2=2Na2CO3+O2↑ |
| 与HCl反应 | Na2O+2HCl=2NaCl+H2O | 2Na2O2+4HCl=4NaCl+2H2O+O2↑ |
| 保存 | 隔绝空气、密封保存 | 隔绝空气、远离易燃物、密封保存 |
其他的常见钠盐:
(1)氯化钠:与硝酸银反应:Cl-+Ag+==AgCl↓
工业上--制碱、生活中--食用、医用上--生理盐水氯化钠(NaCl)
用途:可用于食品调味和腌鱼肉蔬菜;制造氯气、氢气、盐酸、氢氧化钠、氯酸盐、次氯酸盐、漂白粉、金属钠,以及供盐析肥皂和鞣制皮革等。经高度精制的NaCl可用来制造生理盐水等。广泛用于临订治疗和生理实验,如失钠、失水、失血等情况。自然界中有盐矿,大量存在于海水和盐湖中。性质:式量58.44。食盐的主要成份。常见的有白色立方晶体或细小的结晶粉末。密度2.165克/厘米3。熔点801℃。沸点1413℃。味咸。溶于水,显中性。由浓缩海水结晶而制得,也可从天然的盐湖或盐井水制取。
(2)硫化钠:
①硫化钠遇酸反应,产生硫化氢。水溶液呈强碱性,故又称硫化碱。溶于硫黄生成多硫化钠。工业品因含杂质常为粉红、棕红色、土黄色块。有腐蚀性,有毒。在空气中易氧化生成硫代硫酸钠。
②硫化钠吸湿性很强,在100g水中的溶解度为15.4g(10℃),57.3g(90℃)。微溶于乙醇,不溶于乙醚。
③贮存方法:应放置通风、干燥处或石棉棚下。应防止雨淋和受潮。硫化碱潮解性大,又易氧化,容器必须密封。
(3)硫代硫酸钠:
①硫代硫酸钠,又名大苏打、海波,白色粉末,易溶于水。
②常用作照相定影剂
③是碘量法常用的还原剂
④与酸很容易歧化,生成气体和沉淀:Na2S2O3+H2SO4=Na2SO4+S↓+SO2↑+H2O
钠的热点化合物:
叠氮酸钠(NaN3),类似于强碱弱酸盐。
氮化钠(Na3N),类盐,水解生成氢氧化钠和氨气,类似氮化镁、氮化钙、碳化钙等。
过硫化钠(Na2S2),具有类似过氧化钠的结构和化学性质。
高铁酸钠(Na2FeO4),具有强氧化性,还原产物为+3价铁的化合物。
铝盐:
铝盐是指正三价铝离子和酸根阴离子组成的盐,一般来说呈白色或无色晶体,溶于水,个别不溶于水。
常用的铝盐主要有三氯化铝、硫酸铝和明矾。
(1)与碱反应:Al3++3OH-(少量)==Al(OH)3↓
Al3++4OH-(过量)== AlO2-+2H2O
(2)Al3++3AlO2-+6H2O==4Al(OH)3↓
铝盐的性质:
Al3+易水解,显酸性Al3++3H2O==Al(OH)3+3H+
(1)与碱反应:Al3++3OH-(少量)==Al(OH)3↓
Al3++4OH-(过量)==AlO2-+2H2O
(2)易发生双水解:Al3++3AlO2-+6H2O==4Al(OH)3↓
铝盐与强碱溶液作用生成Al(OH)3沉淀的计算
反应关系如下:
(1)Al3++3OH-==Al(OH)3(生成沉淀)
(2)Al(OH)3+OH-==AlO2-+2H2O(沉淀溶解)
(3)Al3++4OH-==AlO2-+2H2O(生成沉淀,又恰好溶解)
分析以上三个化学反应方程式,所得Al(OH)3沉淀的物质的量与n(Al3+)、n(OH-)的关系为:
当 ≤3时,所得沉淀的物质的量:n[Al(OH)3]=
≤3时,所得沉淀的物质的量:n[Al(OH)3]=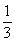 n(OH-)
n(OH-)
当 ≥4时,所得沉淀的物质的量:n[Al(OH)3]=0
≥4时,所得沉淀的物质的量:n[Al(OH)3]=0
当3< <4时,所得沉淀的物质的量:n[Al(OH)3]=4n(Al3+)-n(OH-)
<4时,所得沉淀的物质的量:n[Al(OH)3]=4n(Al3+)-n(OH-)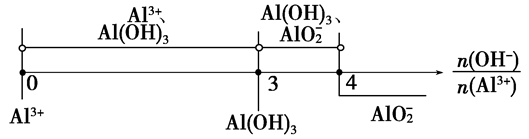
2、有关Al(OH)3的图像分析
①向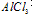 溶液中滴加
溶液中滴加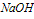 溶液
溶液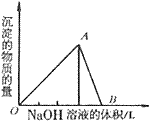
O~A段: 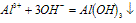
A~B段: 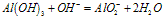
②向强碱溶液中滴入铝盐溶液 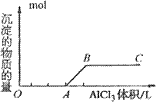
O~A段: 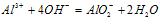
A~B段: 
③向铝盐溶液中滴入氨水或向氨水中滴加铝盐溶液
A. 向铝盐中滴加氨水时,当氨水增加到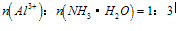 时,产生最大沉淀量
时,产生最大沉淀量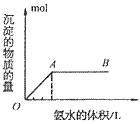
B. 向氨水中滴加铝盐溶液时,开始时氨水过量,如图所示 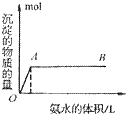
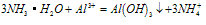
分析得:氢氧化铝不溶于弱碱氨水中。
④向偏铝酸盐溶液中滴入强酸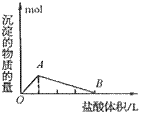
O~A段:
O~B段: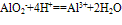
⑤向盐酸中滴加偏铝酸盐溶液 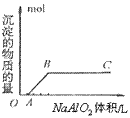
O~A段: 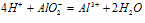
A~B段: 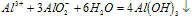
“铝三角”关系:
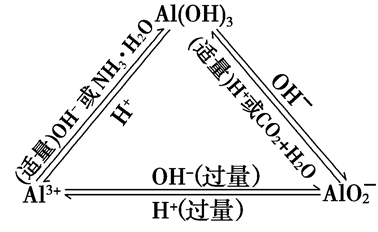
Al3++3OH-===Al(OH)3↓
Al(OH)3+OH-===AlO2-+2H2O
Al3++4OH-===AlO2-+2H2O
AlO2-+2H2O+CO2===Al(OH)3↓+HCO3-
AlO2-+H++H2O===Al(OH)3↓
AlO2-+4H+===Al3++2H2O
典型例题解析:
在50mLbmol·L-1的AlCl3溶液中加入50mLamol·L-1NaOH溶液。
(1)当a≤3b时,生成Al(OH)3沉淀的物质的量为________。
(2)当a、b满足________条件时,无沉淀产生。
(3)当a、b满足________条件时,先有沉淀生成,后又有部分沉淀溶解,此时Al(OH)3的质量为________g。
解析:依题意知,在AlCl3溶液中加入NaOH溶液有如下两个反应发生: AlCl3+3NaOH===Al(OH)3↓+3NaCl ①
AlCl3+4NaOH===NaAlO2+3NaCl+2H2O ②
根据以上两反应可以看出:
(1)当a≤3b时,只发生第一个反应,此时NaOH不足量,产生沉淀的量取决于NaOH。3n[Al(OH)3]=n(NaOH)?。所以答案为0.05a/3mol。
(2)如果无沉淀生成,Al元素全部以AlO2-形式存在。 n(AlCl3)∶n(NaOH)≤1∶4,即a∶b≥4∶1,所以答案为a≥4b。
(3)此种情况应当是两个反应均发生,铝元素以Al(OH)3和AlO2-两种形式存在。符合关系: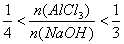 即
即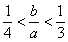 ,整理得:3b<a<4b或
,整理得:3b<a<4b或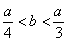 。
。
求沉淀的量的方法很多。
解法一:联立方程法。
设反应①中,AlCl3物质的量为x,则Al(OH)3为x,NaOH为3x。
反应②中AlCl3物质的量为y,NaOH为4y。 
解得x=(0.2b-0.05a)mol=0.05(4b-a)mol。 m[Al(OH)3]=78g·mol-1×0.05(4b-a)mol=3.9(4b-a)g。
解法二:守恒法。此种条件下,溶液中的离子有Na+、Cl-、AlO2-。
n(AlO2-)=n(Na+)-n(Cl-)=0.05amol-0.05×3bmol。
n[Al(OH)3]=n(Al3+)总-n(AlO2-)=0.05bmol-(0.05amol-0.15bmol)=(0.2b-0.05a)mol=0.05(4b-a)mol。
m[Al(OH)3]=78g·mol-1×0.05(4b-a)mol =3.9(4b-a)g。
【答案】 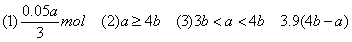
元素性质推断知识点归纳:
(1)质量最轻的元素是氢(H),其单质可以填充气球;质量最轻的金属是锂(Li);熔点最高的非金属单质是石墨;熔点最高的金属单质是钨(W);熔点最低的金属单质是汞(Hg)。
(2)地壳中含量最多是氧(O),其次是Si、Al、Fe、Ca、Na、K、Mg、H、Ti。
(3)既难得电子,又难失电子且为单原子分子的气体是稀有气体。
(4)最高正价与最低负价绝对值之差为4的是硫(S);最高正价与最低负价绝对值之差为零的是碳(C)和硅(Si)。
(5)碳(C)是形成化合物最多的元素,是构成有机物的骨架元素,可形成多种同素异形体,其中硬度最大的是金刚石,而C60是分子晶体,熔点较低。
(6)常温下能与水反应放出氧气,单质是氟(F2),化合物是过氧化钠(Na2O2)。
(7)硅(Si)是构成地壳岩石骨架的主要元素,单质硅可被强碱溶液腐蚀且能放出氢气,还能被弱酸氢氟酸所溶解。
(8)能在空气中自然的非金属单质是白磷(P4),白磷有毒,能溶于CS2,和红磷互为同素异形体,红磷不能自然,不溶于CS2,白磷与红磷在一定的条件下可以相互转化。
(9)既能在二氧化碳中燃烧,又能在氮气中燃烧的金属是Mg,既能与酸溶液又能与碱溶液作用且均放出氢气的金属是铝(Al)。
(10)同一元素的气态氢化物和最高价氧化物的水化物化合生成盐的元素一定是氮(N)。
(11)同一元素的气态氢化物和气态氧化物反应生成该元素得单质和水,该元素可能是氮(N)或硫(S)。
(12)光照时可以释放电子的是铷(Rb)和铯(Cs);常温下呈液态的金属是汞(Hg),非金属单质是溴(Br2)。
解元素推断题必备知识归纳
(1)与元素的原子结构相关知识归纳
①最外层电子数等于次外层电子数的元素是Be、Ar;最外层电子数是次外层电子数2倍的元素有C;最外层电子数是次外层电子数3倍的元素有O;最外层电子数是次外层电子数4倍的元素有Ne。
②次外层电子数是最外层电子数2倍的元素有Li、Si;次外层电子数是最外层电子数4倍的元素有Mg。
③内层电子数是最外层电子数2倍的元素有Li、P;电子总数是最外层电子数2倍的元素有Be。原子核内无中子的元素是11H。
④常见等电子微粒:
|
电子数 |
分子 |
阳离子 |
阴离子 |
|
2 |
H2、He |
Li+、Be2+ |
H- |
|
10 |
Ne、HF、H2O、NH3、CH4 |
Na+、Mg2+、Al3+、H3O+、NH4+ | O2-、F-、OH-、NH2- |
|
18 |
Ar、HCl、H2S、PH3、SiH4、F2、H2O2、N2H4、C2H6、CH3OH |
K+、Ca2+ |
S2-、HS-、Cl- |
①主族序数与周期序数相同的元素有H、Be、Al;主族序数是周期序数2倍的元素有C、S;主族序数是周期序数3倍的元素有O。
②周期序数是主族序数2倍的元素有Li、Ca;周期序数是主族序数3倍的元素有Na。
③最高正价与最低负价的绝对值相等的元素有C、Si;最高正价是最低负价的绝对值3倍的元素有S。
④上一周期元素所形成的阴离子和下一周期元素最高价态阳离子的电子层结构与上一周期零族元素原子的电子层结构相同。
(3)与元素性质相关知识归纳
①元素所形成的单质及化合物的物理特性
A.颜色:常温下,单质为有色气体的元素是F、Cl;单质为淡黄色固体的元素是S;焰色反应火焰呈黄色的元素是Na,呈紫色的元素是K(通过兰色钴玻璃)。
B.状态:常温下,单质呈液态的非金属元素是Br;单质为白色蜡状固体的元素是P。
C.气味:有臭鸡蛋气味的非金属元素是S。
D.熔点:单质熔点最低的金属元素是Hg;熔点最高的金属元素是W。单质熔点最高的非金属元素是C。氢化物熔点最高的非金属元素是O。氧化物熔点最高的非金属元素是Si。
E.硬度:单质为天然物质中硬度最大的元素是C。
F.密度:单质最轻的金属元素是Li;单质最轻的非金属元素是H。
G.溶解性:气态氢化物最易溶于水的元素是N。
H.导电性:单质能导电的非金属元素是C;单质属于半导体材料的是Si。
②元素所形成的单质及化合物的化学特性
A.无正价、无含氧酸的元素是F;单质氧化性最强、其氢化物水溶液可雕刻玻璃的元素是F;气态氢化物稳定性最强的元素是F;最高价氧化物对应的水化物酸性最强的元素是Cl。
B.其两种同素异形体对人类生存都非常重要的元素是O(O3层被称为人类和生物的保护伞);气态氢化物与最低价氧化物能反应生成单质的是S。
C.气态氢化物与最高价氧化物对应水化物能起化合反应的元素是N;气态氢化物能使湿润的红色石蕊试纸变蓝的元素是N;其中一种同素异形体在空气中能自燃的元素是P。
③元素性质递变规律
A.元素金属性强弱比较规律
I.依据元素周期表,同一周期中,从左到右,金属性逐渐减弱;同一主族中,由上到下,金属性逐渐增强。
II.依据最高价氧化物的水化物碱性强弱,碱性越强,金属性越强。
III.依据金属活动性顺序(极少数例外)。
IV.依据金属单质与酸或水反应的剧烈程度,反应越剧烈,金属性越强。
V.依据金属单质与盐溶液之间的置换反应。
VI.依据原电池原理,原电池中作负极的金属比作正极的金属金属性强。
VII.依据电解原理,电解时,阴极上后析出的金属比先析出的金属金属性强。
B.元素非金属性强弱比较规律
I.依据元素周期表,同一周期中,从左到右,非金属性逐渐增强;同一主族中,由上到下,非金属性逐渐减弱。
II.依据最高价氧化物的水化物的酸性强弱,酸性越强,非金属性越强。
III.依据与H2化合的难易,越容易化合,非金属性越强。
IV.依据其气态氢化物的稳定性,稳定性越强,非金属性越强。
V.依据非金属单质与盐溶液之间的置换反应。
C.微粒半径大小比较规律
I.同周期阳离子半径随原子序数递增逐渐减小,如第3周期中:Na+>Mg2+>Al3+;同周期阴离子半径随原子序数递增逐渐减小,如第3周期中:P3->S2->Cl-。
II.同主族阳离子半径随原子序数递增逐渐增大,如第IA族中:Li<Na+<K+,同主族阴离子半径随原子序数递增逐渐增大,如第VIIA族中:F-<Cl-<Br-。
III.阳离子半径总比相应原子半径小,如Na+<Na,阴离子半径总比相应原子半径大,如S2->S。
IV.电子层结构相同的离子半径随原子序数的增大而减小,如S2->Cl->K+>Ca2+,O2->F->Na+>Mg2+>Al3+。
④元素的含量地壳中质量分数最大的元素是O,其次是Si;地壳中质量分数最大的金属元素是Al,其次是Fe;氢化物中氢元素质量分数最大的是C;所形成的有机化合物中种类最多的是C。
(3)解元素推断题的方法解答元素推断题,必须抓住原子结构和元素的有关性质,掌握元素周期表中主要规律,熟悉某些元素(短周期或前20号元素)的性质、存在和用途的特殊性,用分析推理法确定未知元素在周期表中的位置。对于有突破口的元素推断题,可利用题目暗示的突破口,联系其它条件,顺藤摸瓜,各个击破,推出结论。对无明显突破口的元素推断题,可利用题示条件的限定,逐渐缩小推求范围,并充分考虑各元素的相互关系予以推断。有时限制条件不足,则可进行讨论,得出合理结论,有时答案不止一组,只要能解释通都可以,若题目只要求一组,则选择自己最熟悉、最有把握的。有时需要运用直觉,大胆尝试、假设,再根据题给条件进行验证,也可推出。
(1)以铜锌原电池为例:
负极(Zn):Zn-2e-=Zn2+
正极(Cu):2H++2e-=H2↑
(2)正负极反应式的书写技巧:
①先确定原电池的正负极,在两极的反应物上标出相同数目的电子得失。
②根据物质放电后生成物的组成和电解质溶液中存在的离子,找到电极反应中还需要的其它离子。此时要注意溶液的酸碱性,从而判断应该是H+、OH-还是H2O参与了反应。因Zn反应后生成了Zn(OH)2,而KOH为电解质,可知负极上OH-参与了反应。MnO2生成了MnO(OH),即增加了氢元素,可知正极上有水参与了反应。
③根据电子守恒和电荷守恒写出电极反应式,即要注意配平和物质的正确书写形式,应按照离子方程式的书写要求进行。②中反应的电极反应式为:
负极:Zn+2OH--2e-=Zn(OH)2 正极:2MnO2+2H2O+2e-=2MnO(OH)+2OH-
(若只要求写正极的反应式,也可以写成MnO2+H2O+e-=MnO(OH)+OH-)
原电池总反应式的书写:将正负电极反应相加,即为原电池总反应式。
原电池正、负极的判断方法:
原电池有两个电极,一个是正极,一个是负极,判断正极和负极的方法有以下几种。
1.由组成原电池的两极材料判断一般相对较活泼的金属为负极,相对不活泼的金属或能导电的非金属为正极。
2.根据电流方向或电子流动方向判断在外电路,电流由正檄流向负极;电子由负极流向正极
3.根据原电池里电解质溶液中离子的定向移动方向判断在原电池的电解质溶液内,阳离子移向正极,阴离子移向负极。
4.根据原电池两极发生的变化来判断原电池的负极总是失电子发生氧化反应,正极总是得电子发生还原反应。
5.X极增重或减轻工作后,X极质量增加,说明X极有物质析出,X 极为正极:反之,X极质量减少,说明X极金属溶解,X 极为负极
6.X极有气泡冒出工作后,x极上有气泡冒出,一般是发生了析出H,的电极反应,说明x极为正极。
7.X极附近pH的变化析氢或吸氧的电极反应发生后,均能使该电极附近电解质溶液的pH增大,因而工作后,X极附近pH增大了,说明X极为正极。
8.特例在判断金属活泼性的规律中,有一条为“当两种金属构成原电池时,活泼金属作负极,不活泼金属作正极”,但这条规律也有例外情况,如Mg和Al为原电池的两极,KOH为电解质溶液时,虽然Mg比Al活泼,但因Mg不和KOH反应,所以Mg作原电池的正极等。
与“已知X+、Y3+、Z-、W2-是短周期元素X、Y、Z、W形成的离子,甲...”考查相似的试题有:
- 在足量的硫酸铜溶液中分别投入下列物质:①Na;②Na2O2;③Na2O;④NaOH;⑤Na2CO3;⑥Fe,其中实验现象相同,发生反应的类型也相同...
- (6分)某天然碱可以看作是CO2和NaOH反应后的产物组成的一种物质。为了测定该物质的成分,进行如下实验:⑴称取3.32g天然碱样...
- 将11.5 g金属钠投入到88.5 g水中,反应完毕后,求生成溶液的质量分数(不考虑水的蒸发)。
- 将一块部分被氧化的金属钠(假设氧化产物只有Na2O2)投入盛满水且倒置水槽内的容器中,此时在容器中可收集到448mL(标准状况)气...
- 现有NaCl、Na2SO4、NaNO3的混合物,选择适当的试剂将其转化为相应的沉淀和固体,从而实现阴离子的分离。相应的实验过程可用下...
- 将一小块金属钠投入盛少量饱和澄清石灰水的试管里,不可能观察到的现象是A.钠熔成小球并在液面上游动B.有气体生成C.溶液底...
- 下列表述正确的是①开发使用新型清洁能源,减少化石燃料的燃烧,可从根本上防止酸雨的产生 ②我国从2000年起逐渐用二氧化氯取代...
- W、X、Y、Z是周期表前36号元素中的四种常见元素,其原子序数一次增大。W、Y的氧化物是导致酸雨的主要物质,X的基态原子核外有...
- A、B、C、D、E是位于短周期的主族元素,其中A、B为金属元素。已知:①热稳定性:HmD>HmC;②Cm-、E(m-1)-具有相同的电子层结构...
- (10分)美国阿波罗宇宙飞船上使用的氢氧燃料电池是一种新型的化学电池,其构造如图所示;两个电极均由多孔性碳制成,通入的...