本试题 “金属加工后的废切削液中含2%~3%的NaNO2,它是一种环境污染物。人们用NH4Cl溶液来处理废切削液,使NaNO2转化为无毒物质,该反应分两步进行:下列对第二步反应...” 主要考查您对氧化剂、还原剂
分解反应
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 氧化剂、还原剂
- 分解反应
(1)定义:得到电子(或电子对偏向)的物质,在反应时所含元素的化合价降低。
(2)常见的氧化剂:
①活泼非金属单质:如 Cl2、Br2、O2等。
②某些高价氧化物,如SO3、MnO2等。
③氧化性含氧酸,如 浓H2SO4、HNO3、HClO等
④元素(如Mn、Cl、Fe等)处于高化合价时的盐,如KMnO4、K2Cr2O7、KClO3、FeCl3等。
⑤过氧化物,如Na2O2、H2O2等。
⑥某些金属阳离子:如Ag+、Fe3+等
还原剂:
(1)定义:失去电子(或电子对偏离)的物质,在反应时所含元素的化合价升高。
(2)常见的还原剂:
①活泼金属单质:如 Na、A1、Zn、Fe等。
②低价态的金属阳离子:如Fe2+等;
③某些非金属单质:如 H2、C等。
④元素(如C、S等)处于低价时的氧化物,如CO、NO、SO2等。
⑤元素(如Cl、S等)处于低化合价时的氢化物:如 H2S、HCl、HI、NH3等 。
⑥元素(如S、Fe等)处于低化合价时的盐或酸,如Na2SO3、H2SO3、H2C2O4、FeSO4等。
常见的氧化剂及对应的还原产物:
|
氧化剂 |
还原产物 |
| Cl2、ClO- | Cl- |
| KMnO4(H+)、MnO2 | Mn2+ |
| HNO3 | NOx、N2、NH4+ |
| 浓H2SO4 | SO2 |
| Ag+、Fe3+ | Ag、Fe2+ |
| H2O2 | H2O |
常见的还原剂及对应的氧化产物:
|
还原剂 |
氧化产物 |
|
Na、K等金属单质 |
Na+、K+ |
|
某些非金属C、S |
CO2、SO2 |
|
非金属的氢化物CH4、H2S、NH3等 |
CO2、S/SO2、NO |
|
某些低价态的氧化物CO、SO2 |
CO2、SO3 |
|
某些低价态的酸或盐H2SO3、Na2SO3等 |
SO42- |
|
某些低价态的阳离子Fe2+ |
Fe3+ |
|
H2O2 |
O2 |
易错易混点:
(1)金属单质只具有还原性,金属最高价阳离子只具有氧化性,处于中间价态的物质既有氧化性,又有还原性;
(2)非金属单质常作氧化剂,某些非金属单质也是较强的还原性物质,比如H2、C等等
(3)元素化合价的变化:
①元素最低价只有还原性,最高价只有氧化性,中间价态既有氧化性又有还原性
②同一元素在反应中化合价发生变化,只能接近不能交叉。
例如: 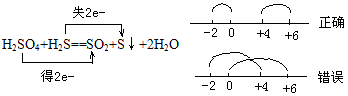
分解反应:
一种化合物在特定条件下(如加热、通直流电、催化剂等)分解成两种或两种以上较简单的单质或化合物的反应
分解反应类型:
氧化物分解: 2H2O=(通电)2H2↑+O2↑ 2H2O2=(MnO2)2H2O+O2↑
含氧酸分解: H2CO3=(△)H2O+CO2↑ H2SO3=(△)H2O+SO2↑
碱的分解: Mg(OH)2=(高温)MgO+H2O Cu(OH)2=(△)CuO+H2O 2Fe(OH)3=(高温)Fe2O3+3H2O
2Al(OH)3=(高温)Al2O3+3H2O (注:不溶性碱高温时可分解为金属氧化物和水)
盐的分解: 2NaHCO3=(△)Na2CO3+CO2↑+H2O Ca(HCO3)2=(△)CaCO3+CO2↑+H2O CaCO3=(高温)CaO+CO2↑
2KMnO4=(△)K2MnO4+MnO2+O2↑ 2KClO3=(△,MnO2)2KCl+3O2↑
分解反应的模型:
A=B+C 可以简单理解为“一变多”,也可以理解成为由一种反应物发生化学反应后生成两种或两种以上的物质的反应。
分解反应与氧化还原反应的关系:
分解反应不一定是氧化还原反应,例如:2Al(OH)3=(高温)Al2O3+3H2O
只有能产生单质的分解反应才是氧化还原反应,例如:2H2O=(通电)2H2↑+O2↑
与“金属加工后的废切削液中含2%~3%的NaNO2,它是一种环境污染物...”考查相似的试题有:
- 以下转化需加入还原剂才能实现的是[ ]A.Al(OH)3→Al2O3B.Cu→CuCl2C.FeCl2→FeD.Na→NaOH
- 下列试剂在空气中易被氧化而变质的是( )A.Na2O2B.Na2CO3C.CuCl2D.FeSO4
- KClO3和浓盐酸在一定温度下反应会生成黄绿色的 易爆物二氧化氯。其变化可表示为:2KClO3+4HCl(浓)=2KCl+2ClO2↑+Cl2↑+2H2O。(1...
- 有氰化物的废水危害极大,能毒杀各种鱼类和水生生物。CN-浓度在0. 01~0. 04 mg·L-1时就有强烈的毒杀作用,处理含有氰化物的...
- 下列微粒只具有氧化性的是( )A.Fe2+B.Fe3+C.COD.Cu
- 下列微粒中,只有氧化性的是[ ]①S2-②Fe2+③Fe3+④S ⑤H+⑥Na+⑦MgA.①⑦B.②④C.③⑤⑥D.②④⑤⑥
- 实验室常用NaNO2和NH4Cl反应制取N2。下列有关说法正确的是[ ]A.NaNO2是还原剂B.NH4Cl中N元素被还原C.生成1 mol N2时转移6 ...
- 纳米技术是正在崛起的新科技,它研究的粒子直径在l~100nm之间。在此范围内物质的性质发生很大变化。例如Cu的直径加工成几个...
- A、B、C、D是由前18号元素组成的四种常见化合物,D为红棕色气体,甲、乙是两种单质,这些单质和化合物之间存在如下反应关系(...
- 如图所示,2个X分子反应生成1个Y分子和3个Z分子,下列判断不正确的是:[ ]A.根据质量守恒定律可推知,1个Z分子中含有2个同种...