本试题 “现在有一种含氧酸盐的固体试样,经测定,该固体含2种金属元素和两种非金属元素。其中酸根由一种金属元素和氧元素组成,且两种元素质量比为7:8。为进一步确定...” 主要考查您对铁盐(三价铁离子)
硫酸盐
金属、非金属的有关计算
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 铁盐(三价铁离子)
- 硫酸盐
- 金属、非金属的有关计算
Fe3+的性质:
含Fe3+的溶液都呈黄色,具有氧化性,
(1)与还原剂反应生成二价铁 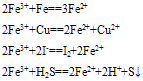
(2)与碱反应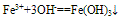
(3)Fe3+在水中易水解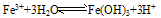
由于三价铁易水解,在保存铁盐盐溶液(FeCl3)时加入少量相应的酸(HCl),以防止Fe3+水解。
“铁三角”中的转化关系:
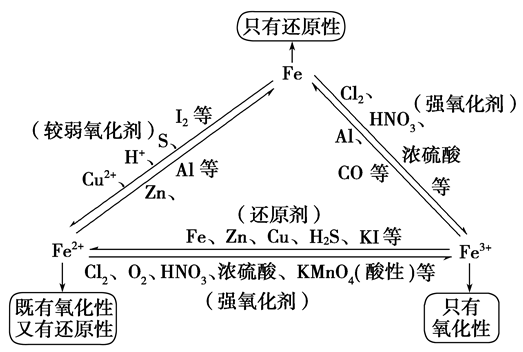
几种重要的硫酸盐:

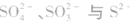 的检验:
的检验:
1.SO42-的检验
(1)原理:利用 ,
,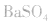 具有不溶于盐酸、硝酸的特性。
具有不溶于盐酸、硝酸的特性。
(2)试剂:可溶性钡盐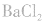 溶液或
溶液或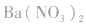 溶液,盐酸和稀硝酸。
溶液,盐酸和稀硝酸。
(3)易出现的错误:
①只加可溶性钡盐,不酸化。误将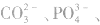 、
、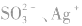 等判成SO42-,此时上述离子会分别产生
等判成SO42-,此时上述离子会分别产生 等白色沉淀.
等白色沉淀.
②先加可溶性盐,后酸化。误将 等判成SO42-,如向待测液中先滴加
等判成SO42-,如向待测液中先滴加 溶液,再加盐酸有白色沉淀生成便断定含SO42-。其错误之处是未注意溶液中不含SO42-而含Ag+或
溶液,再加盐酸有白色沉淀生成便断定含SO42-。其错误之处是未注意溶液中不含SO42-而含Ag+或 也会有同样现象,因为
也会有同样现象,因为
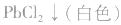
③试剂选择错误。误将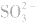 判成
判成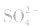 ,如向待测液中滴加盐酸酸化的
,如向待测液中滴加盐酸酸化的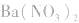 溶液,或滴加硝酸酸化的
溶液,或滴加硝酸酸化的 溶液,生成白色沉淀,使误以为有
溶液,生成白色沉淀,使误以为有 ,错在未注意
,错在未注意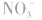 在酸性条件下具有强氧化性,可将
在酸性条件下具有强氧化性,可将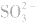 氧化成
氧化成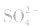 。
。
(4)检验的关键:既要注意试刹的选择,义耍注意操作顺序的优化,全面考虑,综合分析,正确推导,方能排除干扰离子。
(5)最佳检验方法:
2.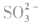 的检验常用气体法:
的检验常用气体法: (不能用硝酸等强氧化性酸),生成能使品红溶液褪色的无色有刺激性气味的气体。
(不能用硝酸等强氧化性酸),生成能使品红溶液褪色的无色有刺激性气味的气体。
3. 的检验
的检验
(1)气体法: ,所用酸必须是非强氧化性酸,可用稀盐酸或稀硫酸,生成能使湿润的醋酸铅试纸变黑的气体。
,所用酸必须是非强氧化性酸,可用稀盐酸或稀硫酸,生成能使湿润的醋酸铅试纸变黑的气体。
(2)沉淀法: ,生成黑色沉淀;或
,生成黑色沉淀;或 ,生成乳白色或黄色沉淀(溶液中)。
,生成乳白色或黄色沉淀(溶液中)。
亚硫酸及亚硫酸盐:
1.亚硫酸溶液中的微粒
SO2与水反应生成亚硫酸,亚硫酸不稳定,易分储成SO2和H2O,因此SO2与H2O的反应是一个可逆反应,用“ ”表示。
”表示。 
在亚硫酸溶液中存在的微粒有(三分子、四离子):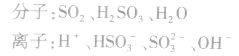
2.亚硫酸的性质
(1)亚硫酸的热稳定性
H2SO3极其不稳定,只能存在于稀的水溶液中。 H2SO3易分解生成SO2和H2O。 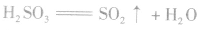
(2)亚硫酸的氧化性和还原性
H2SO3遇到比它更强的氧化剂时,表现还原性。如:
H2SO3遇到比它更强的还原剂时,表现氧化性。如:
(3)亚硫酸的酸性
H2SO3是中强酸,在水溶液中分两步电离: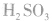
 。
。
由亚硫酸的组成和电离可知,亚硫酸对应的盐有正盐和酸式盐两种,如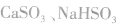 。
。
3.亚硫酸盐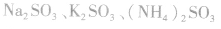 等亚硫酸盐易溶于水、易电离。
等亚硫酸盐易溶于水、易电离。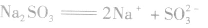

包括金属及化合物、金属与非金属化合物、非金属化合物之间的反应的计算,解此类题的关键是正确的写出反应方程式,明确物质间的等量关系。明确物质之间的反应,正确写出方程式,此类题可迎刃而解。
AlCl3与NaOH反应的相关计算:
1、求Al(OH)3沉淀的量
2、求反应物碱的量
铝与酸、碱反应的计算规律:
铝分别与盐酸、氢氧化钠溶液反应的原理: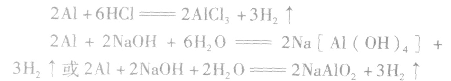
(1)等量铝分别与足量盐酸和氢氧化钠溶液反应,产生氢气的体积比为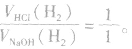
(2)足量的锅分别与等物质的量的盐酸和氢氧化钠溶液反应,产生氢气的体积比为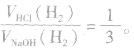
(3)一定量的铝分别和一定量的盐酸和氢氧化钠溶液反应,若产生氢气的体积比为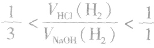 ,则必定是:
,则必定是:
①铝与盐酸反应时,铝过量而盐酸不足;
②铝与氢氧化钠溶液反应时,铝不足而氢氧化钠过量。
解有关硝酸与金属反应的计算题的技巧:
1.灵活运用得失电子守恒、原子守恒及溶液中的电荷守恒关系例如Cu与HNO3反应中就有以下等量关系:
(1)N原子守恒:反应前所有的N只存在于HNO3中;反应后含N的物质有HNO3的还原产物(假设此处有NO3、NO)和Cu(NO3)3,若HNO3过量,则过量HNO3中也含一部分N,则有:n(N)=n(NO2)+ n(NO)+2n[Cu(NO3)3]+n剩(HNO3)。
(2)得失电子守恒:在反应中失去电子的是参加反应的Cu, ;得到电子的是被还原的HNO3(假设还原产物为NO2、NO),NO3-+e→ NO2、NO3-+3e→NO。根据得失电子守恒,则有:
;得到电子的是被还原的HNO3(假设还原产物为NO2、NO),NO3-+e→ NO2、NO3-+3e→NO。根据得失电子守恒,则有: 
(3)溶液中的电荷守恒:在任何溶液中,阴离子所带负电荷总数与阳离子所带正电荷总数在数值上是相等的。在Cu与HNO3反应后的溶液中,若HNO3不过量,阳离子只有Cu2+,阴离子只有NO3-(此类计算不考虑H2O电离出的极少量的H+、OH-);若HNO3过量,溶液中阳离子有Cu2+和H+,阴离子只有NO3-。则有:
①若HNO3不过量: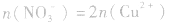
②若HNO3过量: 
2.铁与稀HNO3的反应规律 

(2)上述反应可以认为先发生反应①,若Fe有剩余则发生 ①×2+ ③即得反应②,所以,无论是反应①还是反应②,被还原的HNO3皆占参加反应的HNO3的
①×2+ ③即得反应②,所以,无论是反应①还是反应②,被还原的HNO3皆占参加反应的HNO3的 。
。
有关镁、铝的图像集锦:
Al(OH)3与Al3+、AlO2-之间的转化,是建立在 Al(OH)3两性基础上的,有关相互转化的配比和沉淀Al(OH)3的质量变化,见下表:
与“现在有一种含氧酸盐的固体试样,经测定,该固体含2种金属元素...”考查相似的试题有:
- 下列反应中,观察不到颜色变化的是( ) A.黄色的氯化铁溶液中加入足量铁粉 B.往稀硫酸中通入氨气 C.往品红溶液中通入足量...
- 下列化合物中,不能通过两种单质直接化合制取的是[ ]A.FeCl3B.CuCl2C.HClD.FeCl2
- 氧化还原反应在工农业生产和日常生活中有广泛运用(1)人通过呼吸作用吸入氧气,氧化体内的葡萄糖(C6H12O6)提供能量以维持...
- 将1.12g铁粉加入25mL 2mol•L-1的氯化铁溶液中,充分反应后,其结果是( ) A.铁有剩余,溶液呈浅绿色,Cl-浓度基本不变 B....
- 氮化铁磁粉是一种磁记录材料,利用氨气在400℃以上分解,将分解的氮原子渗透到铁粉中制备氮化铁。下面是制备氮化铁的步骤:(1)...
- 把ag 铝铁合金粉末溶于足量盐酸中,再加入过量氢氧化钠溶液。过滤出沉淀,经洗涤、干燥、灼烧,得到红棕色粉末的质量仍为ag,...
- 氯化亚铜(CuCl)是重要的化工原料。国家标准规定合格的CuCl产品的主要质量指标为CuCl的质量分数大于96.5%。工业上常通过下列反...
- 1 L某混合溶液,可能含有的离子如下表:(1)往该溶液中逐滴加入NaOH溶液并适当加热,产生沉淀和气体的物质的量()与加入NaOH...
- 有相同质量的两份NaHCO3粉末,第一份加入足量盐酸,第二份先加热使其完全分解再加足量同质量分数的盐酸,则两者所消耗的盐酸...
- 盐酸、硫酸和硝酸是中学阶段常见的三种强酸。请就三者与金属铜的反应情况,回答下列问题(1) ①在100mL 18 mol/L的浓硫酸中加...