本试题 “请回答下列问题.(1)水中存在平衡:H2O⇌H++OH-△H>0,欲使平衡右移,且溶液显酸性,可选的方法是______.(选填序号)a.向水中加入NaHSO4固体 b.向水中加...” 主要考查您对水电离的影响因素
水的电离平衡
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 水电离的影响因素
- 水的电离平衡
影响水电离平衡的因素:
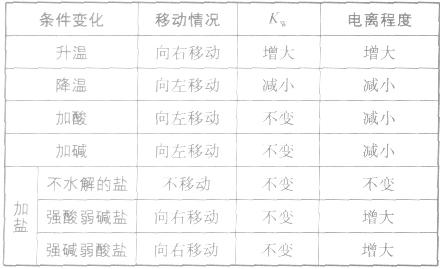
水的电离:
水是一种极弱的电解质,可以发生微弱电离,电离方程式为:H2O H++OH-。25℃时,水电离出来的c(H+)=c(OH-)=10-7mol/L
H++OH-。25℃时,水电离出来的c(H+)=c(OH-)=10-7mol/L
注:水的电离是永恒存在的,不研究水溶液的体系中均存在水的电离平衡,不要忽略H+和OH-共同存在。
水是一种极弱的电解质,可以发生微弱电离,电离方程式为:H2O
 H++OH-。25℃时,水电离出来的c(H+)=c(OH-)=10-7mol/L
H++OH-。25℃时,水电离出来的c(H+)=c(OH-)=10-7mol/L 注:水的电离是永恒存在的,不研究水溶液的体系中均存在水的电离平衡,不要忽略H+和OH-共同存在。
发现相似题
与“请回答下列问题.(1)水中存在平衡:H2O⇌H++OH-△H>0,欲使...”考查相似的试题有:
- 室温下,一元酸HA溶液与一元碱BOH溶液等体积混合,下列有关判断正确的是A.若混合后所得溶液呈中性,则HA肯定是强酸、BOH肯定...
- (5分)日常生活中,可用明矾[KAl(SO4)2·12H2O]作为净水剂,这是因为:明矾溶于水发生水解反应,生成氢氧化铝胶体。(1)该反应...
- 在下列各微粒中,能使水的电离平衡向正方向移动,而且溶液的pH小于7是
- 常温下,下列各溶液中微粒的物质的量浓度关系正确的是A.某物质的溶液pH < 7,则该物质一定是酸或强酸弱碱盐B.AgCl在同浓度...
- (9分)计算0.01mol/LHCl溶液PH值?在此溶液中由水电离出的c(H+)是多少?若将此酸50ml与50ml 0.012mol/LNaOH混合,溶液中的...
- T°C时,将体积为VAL、浓度为a mol/L的一元酸HA与体积为VBL、浓度为b mol/L的一元碱BOH混合,混合液恰好呈中性,则下列判断正...
- 25℃时,1L0.01mol/LHCl溶液,水的离子积常数Kw为______,溶液中H+的物质的量浓度为______,水电离出的H+的物质的量浓度为____...
- 标准状况下,一个装满O2的容器的质量为79g,若装满氮气时质量是71g,盛满某气体X时,质量为103g。试计算:⑴此容器的容积⑵气体...
- 下列关系正确的是A.常温下,pH=3强酸HA溶液与pH=11NaOH溶液混合,c(Na+)= c(A-)>c(H+)= c(OH-)B.c(NH4+)相等的①(NH4)2SO...
- 用稀盐酸预处理强酸型阳离子交换树脂,使之变为HR,再用蒸馏水洗涤至中性,然后用该树脂软化100mL含0.001molMg2+的中性溶液,...