本试题 “工业上用丁烷氧化法制醋酸,反应的化学方程式可表示为:2C4H10+5O2一定条件4CH3COOH+2H2O,现用58吨丁烷为原料制取醋酸,求:(1)理论上需要标准状况下的空...” 主要考查您对化学反应方程式
溶液质量分数的计算
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 化学反应方程式
- 溶液质量分数的计算
化学方程式:
用化学式来表示化学反应的式子,叫做化学方程式。化学方程式不仅表明了反应物、生成物和反应条件,同时,通过相对分子质量或相对原子质量还可以表示个物质之间的质量关系,即各物质之间的质量比。
书写化学方程式要遵守两个原则:
一是必须以客观事实为基础,绝不能凭空臆想、臆造事实上不存在的物质和化学反应;
二是要遵守质量守恒定律,等号两边各原子种类与数目必须相等。
化学方程式的意义:
化学方程式不仅表明了反应物、生成物和反应条件。同时,化学计量数代表了各反应物、生成物物质的量关系,通过相对分子质量或相对原子质量还可以表示各物质之间的质量关系,即各物质之间的质量比。对于气体反应物、生成物,还可以直接通过化学计量数得出体积比。
溶液质量分数的计算:
(1)溶质的质量分数=
(2)溶质的质量分数、溶质的物质的量浓度及溶液密度之间的关系:
①溶质的质量分数=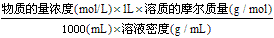
②物质的量浓度=
(1)溶质的质量分数=

(2)溶质的质量分数、溶质的物质的量浓度及溶液密度之间的关系:
①溶质的质量分数=
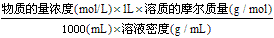
②物质的量浓度=

有关溶液密度的问题:
1.溶液质量分数与密度的关系
(1)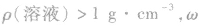 越大,则ρ(溶液)越大,常见溶液如NaCl溶液、硫酸溶液等。
越大,则ρ(溶液)越大,常见溶液如NaCl溶液、硫酸溶液等。
(2)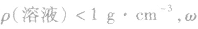 越大,则ρ(溶液)越小,常见溶液如氨水、酒精溶液等。
越大,则ρ(溶液)越小,常见溶液如氨水、酒精溶液等。
2.溶液混合后质量分数的变化规律
质量分数分别为 的两溶液(同种溶质)混合,混合后溶液的质量分数为ω。
的两溶液(同种溶质)混合,混合后溶液的质量分数为ω。
(1)等体积混合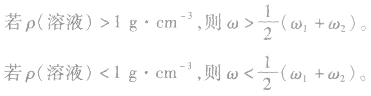
若是加等体积水稀释,可视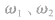 中其一为0 分析。
中其一为0 分析。
(2)等质量混合: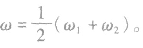
发现相似题
与“工业上用丁烷氧化法制醋酸,反应的化学方程式可表示为:2C4H1...”考查相似的试题有:
- 为测定某氯水的物质的量浓度,取100mL氯水,加入足量的碘化钾溶液充分反应,然后用300ml 1mol/L硫代硫酸钠(Na2S2O3)溶液恰...
- 质量相同的下列烃,完全燃烧,耗氧量最多的是( ) A.C2H6 B.C4H6 C.C5H10 D.C7H8
- 已知一定条件下碳碳双键可被酸性KMnO4溶液氧化,羰基可以与乙炔发生加成反应.现有化合物A的一系列反应(反应条件略去),其...
- 写出5个有CO2生成,且符合下列要求的化学方程式:(1)一种盐分解___;(2)一种金属氧化物跟单质反应___;(3)一种非金属氧化物跟...
- 在实验室中,氮氧化物废气(主要成分NO2和NO)可以用NaOH溶液来吸收,以除去这些废气,其主要反应为:2NO2+2NaOH→NaNO2+NaNO3...
- 已知A 是一种分子量为28的气态烃,现以A为主要原料合成一种具有果香味的物质E,其合成路线如下图所示.请回答下列问题:(1)...
- 20℃时,饱和KCl溶液的密度为1.174g•cm-3,物质的量浓度为4.0mol•L-1,则下列说法中正确的是( )A.25℃时,饱和KCl溶液的浓度...
- 已知NH3和HCl都能用来作喷泉实验的气体,若在同温同压下用等体积烧瓶各收集满NH3和HCl气体,实验后两个烧瓶内溶液的关系是(...
- 将37.2gNa、Na2O、Na2O2组成的混合物放入盛有206.4mL水(密度为1.0g/cm3)的特定容器中充分反应,将反应后产生的气体全部收集...
- 若以w1和w2分别表示浓度为amol·L-1和 bmol·L-1氨水的质量分数,且知2a=b,则下列推断正确的是(氨水的密度比纯水的小)[ ]A....