本试题 “已知:铅蓄电池总的化学方程式为:Pb+PbO2+2H2SO42H2O+2PbSO4;镍镉碱性充电电池在放电时,其正极反应为:2NiO(OH)+2H2O+2e-=2Ni(OH)2+2OH-负极反应为:Cd...” 主要考查您对原电池电极反应式的书写
二次电池
电解池电极反应式的书写
电化学有关的计算
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 原电池电极反应式的书写
- 二次电池
- 电解池电极反应式的书写
- 电化学有关的计算
(1)以铜锌原电池为例:
负极(Zn):Zn-2e-=Zn2+
正极(Cu):2H++2e-=H2↑
(2)正负极反应式的书写技巧:
①先确定原电池的正负极,在两极的反应物上标出相同数目的电子得失。
②根据物质放电后生成物的组成和电解质溶液中存在的离子,找到电极反应中还需要的其它离子。此时要注意溶液的酸碱性,从而判断应该是H+、OH-还是H2O参与了反应。因Zn反应后生成了Zn(OH)2,而KOH为电解质,可知负极上OH-参与了反应。MnO2生成了MnO(OH),即增加了氢元素,可知正极上有水参与了反应。
③根据电子守恒和电荷守恒写出电极反应式,即要注意配平和物质的正确书写形式,应按照离子方程式的书写要求进行。②中反应的电极反应式为:
负极:Zn+2OH--2e-=Zn(OH)2 正极:2MnO2+2H2O+2e-=2MnO(OH)+2OH-
(若只要求写正极的反应式,也可以写成MnO2+H2O+e-=MnO(OH)+OH-)
原电池总反应式的书写:将正负电极反应相加,即为原电池总反应式。
原电池正、负极的判断方法:
原电池有两个电极,一个是正极,一个是负极,判断正极和负极的方法有以下几种。
1.由组成原电池的两极材料判断一般相对较活泼的金属为负极,相对不活泼的金属或能导电的非金属为正极。
2.根据电流方向或电子流动方向判断在外电路,电流由正檄流向负极;电子由负极流向正极
3.根据原电池里电解质溶液中离子的定向移动方向判断在原电池的电解质溶液内,阳离子移向正极,阴离子移向负极。
4.根据原电池两极发生的变化来判断原电池的负极总是失电子发生氧化反应,正极总是得电子发生还原反应。
5.X极增重或减轻工作后,X极质量增加,说明X极有物质析出,X 极为正极:反之,X极质量减少,说明X极金属溶解,X 极为负极
6.X极有气泡冒出工作后,x极上有气泡冒出,一般是发生了析出H,的电极反应,说明x极为正极。
7.X极附近pH的变化析氢或吸氧的电极反应发生后,均能使该电极附近电解质溶液的pH增大,因而工作后,X极附近pH增大了,说明X极为正极。
8.特例在判断金属活泼性的规律中,有一条为“当两种金属构成原电池时,活泼金属作负极,不活泼金属作正极”,但这条规律也有例外情况,如Mg和Al为原电池的两极,KOH为电解质溶液时,虽然Mg比Al活泼,但因Mg不和KOH反应,所以Mg作原电池的正极等。
(1)蓄电池:蓄电池是可以反复使用、放电后可以充电使活性物质复原、以便再重新放电的电池,也称二次电池。其广泛用于汽车、发电站、火箭等部门。由所用电解质的酸碱性质不同分为酸性蓄电池和碱性蓄电池。
①酸性铅蓄电池铅蓄电池由一组充满海绵状金属铅的铅锑合金格板做负极,由另一组充满二氧化铝的铅锑合金格板做正极,两组格板相间浸泡在电解质稀硫酸中,放电时,电极反应为:
负极:Pb+SO42-=PbSO4+2e- 正极:PbO2+SO42-十4H++2e-=PbSO4+2H2O
总反应:Pb+PbO2+2H2SO4=2PbSO4十2H2O
放电后,正负极板上都沉积有一层PbSO4,放电到一定程度之后又必须进行充电,充电时用一个电压略高于蓄电池电压的直流电源与蓄电池相接,将负极上的PbSO4还原成Pb,而将正极上的PbSO4氧化成PbO2,
充电时发生放电时的逆反应:阴极:PbSO4+2e-=Pb+SO42-阳极:PbSO4+2H2O=PbO2+SO42-+4H++2e- 总反应:2PbSO4+2H2O=Pb+PbO2+H2SO4
②碱性蓄电池日常生活中用的充电电池就属于这类。它的体积、电压都和干电池差不多,携带方便,使用寿命比铅蓄电池长得多,使用信当可以反复充放电上千次,但价格比较贵。商品电池中有镍-镉(Ni-Cd)和镍一铁(Ni-Fe)两类,它们的电池反应是:
Cd+2NiO(OH)+2H2O
 2Ni(OH)2+Cd(OH)2
2Ni(OH)2+Cd(OH)2 Fe+2NaO(OH)+2H2O
 2Ni(OH)2+Fe(OH)2
2Ni(OH)2+Fe(OH)2 反应是在碱性条件下进行的,所以叫碱性蓄电池。
(2)银锌蓄电池 银锌电池是一种高能电池,它质量轻、体积小,是人造卫星、宇宙火箭、空间电视转播站等的电源。目前,有一种类似干电池的充电电池,它实际是一种银锌蓄电池,电解液为KOH溶液。 常见的钮扣电池也是银锌电池,它用不锈钢制成一个由正极壳和负极盖组成的小圆盒,盒内靠正极盒一端充由Ag2O和少量石墨组成的正极活性材料,负极盖一端填充锌汞合金作负极活性材料,电解质溶液为KOH浓溶液,溶液两边用羧甲基纤维素作隔膜,将电极与电解质溶液隔开。
负极:Zn+2OH--2e-=Zn(OH)2
正极:Ag2O+H2O+2e-=2Ag+2OH-?
银锌电池跟铅蓄电池一样,在使用一段时间后就要充电,充电过程表示如下:
阳极:2Ag+2OH--2e-=Ag2O+H2O
阴极:Zn(OH)2+2e-=Zn+2OH-?
总反应式:Zn+Ag2O+H2O
 Zn(OH)2+2Ag
Zn(OH)2+2Ag 一粒钮扣电池的电压达1.59V,安装在电子表里可使用两年之久。
1.根据装置书写电极反应式
(1)根据电源确定阴、阳两极→确定阳极是否是活性电极→据电极类型及电解质溶液中阴、阳离子的放电顺序写出电极反应式。
(2)在确保阴、阳两极转移电子数目相同的条件下,将两极电极反应式合并即得总反应式。
2.由氧化还原反应方程式书写电极反应式
(1)找出发生氧化反应和还原反应的物质→确定两极名称和生成物→利用电子守恒分别写出两极反应式。
(2)若写出一极反应式,而另一极反应式不好写,可用总反应式减去已写出的电极反应式,即得另一电极反应式。
电化学计算的基本方法和技巧:
原电池和电解池的计算包括两极产物的定量计算、溶液的pH计算、相对原子质量的计算,根据电量求产物的量或根据产物的量求电量等。通常有下列三种方法。
1.根据电子守恒法
计算用于串联电路中阴、阳两极产物或正、负两极产物的量的计算,其依据是电路中转移的电子数相等。
2.根据总反应式计算
先写出电极反应式,再写出总反应式,最后根据总反应式列比例式计算。
3.根据关系式计算
运用得失电子守恒建立已知量与未知量之间的关系式。如以通过4mole一为桥梁可构建电极产物之间的如下关系式: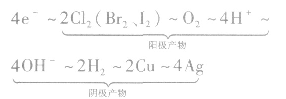
该关系式具有总揽电化学计算的作用和价值,熟记电极反应式,灵活运用这个关系式便能快速解答常见的电化学计算问题。
特别提醒:在电化学计算中,还常利用 和
和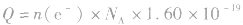 来计算电路中通过的电量。
来计算电路中通过的电量。
与“已知:铅蓄电池总的化学方程式为:Pb+PbO2+2H2SO42H2O+2PbSO4...”考查相似的试题有:
- (1)画出磷原子的原子结构示意图:___________。(2)写出H2S分子的电子式:___________。(3)写出表示含有8个质子,10个中...
- 一种新型燃料电池,以镍板为电极插入KOH溶液中,分别向两极通入乙烷和氧气。有关此电池的推断错误的是A.正极反应为O2+4e-+2...
- 甲醇是一种可再生能源,具有广泛的开发和应用前景。(1)工业上一般采用下列两种反应合成甲醇:反应I:CO(g)+2H2(g)CH3OH(g) △H...
- 将两个铂电极插入KOH溶液中,向两极分别通入CH4和O2,即构成CH4燃料电池.已知通入CH4的一极,其电极反应式是:CH4+10OH--8e-...
- “阿波罗号飞船”所用的氢氧燃料电池的电极应为:负极:2H2+4OH--4e-=4H2O则正极反应为______,该电池工作时,通氢气的一极发生...
- 甲、乙两池的电极材料都是铁棒与碳棒(如下图)。请回答下列问题(1)若两池中均盛放CuSO4溶液,反应一段时间后:①有红色物质析出...
- 下列关于电解质溶液的叙述正确的是A.中和pH与体积都相同的盐酸和硫酸,消耗NaOH的物质的量之比是1∶2B.pH=13的氨水加水稀释...
- 某同学按图示装置进行实验:A极是铜锌合金,B极为纯铜,溶液为足量的硫酸铜溶液。通电一段时间后,若A极恰好全部溶解,此时B...
- .在25℃时,将两个铜电极插入一定质量的硫酸钠的饱和溶液中进行电解。通电一段时间后,阴极是逸出a mol气体,同时有Wg Na2SO4...
- 请从下图中选出必要的装置进行电解饱和食盐水的实验,要求测定产生的H2的体积(大于25 mL),并检验Cl2的氧化性。(1)A极发生...