本试题 “下列过程中,涉及化学变化的是[ ]A.蒸馏法将海水淡化为饮用水B.四氯化碳萃取碘水中的碘C.过滤除去粗盐中的不溶性杂质D.三氯化铁溶液滴入沸水中制胶体” 主要考查您对过滤
碘的萃取
海水资源的综合利用
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 过滤
- 碘的萃取
- 海水资源的综合利用
过滤:
| 名称 | 用途 | 装置 | 举例 | 注意事项 |
| 过滤 | 分离固体和液体混合物 | 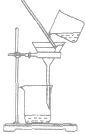 |
粗盐提纯时把粗盐溶于水,经过滤把不溶于水的杂质除去 | ①要“一贴二低三靠” 滤纸紧贴漏斗内壁;滤纸边缘低于漏斗口,漏斗里液面低于滤纸边缘;烧杯口紧靠玻璃棒,玻璃捧下端紧靠三层滤纸.漏斗下端紧靠烧杯内壁。 ②必要时洗涤沉淀物(在过滤器中加少量水),不可搅拌 |
碘的萃取:
(1)现象:静置后,溶液分层,上层为水溶液,无色;下层为四氯化碳的碘溶液,呈紫红色。
(2)原理:水与四氯化碳对比,碘更易溶于四氯化碳
(3)步骤:
①用量筒量取10mL碘的饱和水溶液,倒入分液漏斗,然后再注入4mL四氯化碳,盖好玻璃塞。
②用右手压住分液漏斗口部,左手握住活塞部分,把分液漏斗倒转过来振荡,使两种液体充分接触,振荡后打开活塞,是漏斗内气体放出。
③将分液漏斗放在铁架台上,静置。
④待液体分层后,将分液漏斗颈上的玻璃塞打开,或使塞上的凹槽(或小孔)对准漏斗上的小孔,再将分液漏斗下面的活塞拧开,使下层液体慢慢沿烧杯壁而流下。
(1)现象:静置后,溶液分层,上层为水溶液,无色;下层为四氯化碳的碘溶液,呈紫红色。
(2)原理:水与四氯化碳对比,碘更易溶于四氯化碳
(3)步骤:
①用量筒量取10mL碘的饱和水溶液,倒入分液漏斗,然后再注入4mL四氯化碳,盖好玻璃塞。
②用右手压住分液漏斗口部,左手握住活塞部分,把分液漏斗倒转过来振荡,使两种液体充分接触,振荡后打开活塞,是漏斗内气体放出。
③将分液漏斗放在铁架台上,静置。
④待液体分层后,将分液漏斗颈上的玻璃塞打开,或使塞上的凹槽(或小孔)对准漏斗上的小孔,再将分液漏斗下面的活塞拧开,使下层液体慢慢沿烧杯壁而流下。
海水资源的综合利用:
浩瀚的海洋是个巨大的资源宝库,它不仅孕育着无数的生命,还孕育着丰富的矿产,而海水本身含有大量的化学物质,又是宝贵的化学资源。可从海水中提取大量的食盐、镁、溴、碘、钾等有用物质,海水素有“液体工业原料”之美誉。
浩瀚的海洋是个巨大的资源宝库,它不仅孕育着无数的生命,还孕育着丰富的矿产,而海水本身含有大量的化学物质,又是宝贵的化学资源。可从海水中提取大量的食盐、镁、溴、碘、钾等有用物质,海水素有“液体工业原料”之美誉。
海水制盐:
(1)海水制盐的方法:从海水中得到食盐的方法有蒸发法(盐田法)、电渗析法等。目前,以蒸发法(盐田法)为主。
(2)海水晒盐的基本原理:水分不断蒸发,氯化钠等盐结晶析出。
(3)海水晒盐的流程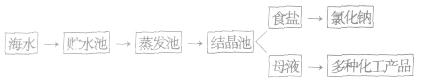
氯碱工业:
(1)食盐水的精制
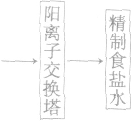
(2)电极反应
阴极: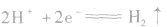
阳极:
总反应: :
:
(3)主要设备
离子交换膜电解槽一一阳极用金属钛(表面涂有钛、钉氧化物层)制成,阴极用碳钢(覆有镍镀层)制成。阳离子膜具有选择透过性,只允许Na+透过,而Cl-、 OH一和气体不能透过。 
(4)产品及用途
烧碱:可用于造纸、玻璃、肥皂等工业
氯气:可用于制农药、有机合成、氯化物的合成
氢气:可用于金属冶炼、有机合成、盐酸的制取
海水提溴:
(1)氯化
氯化氧化溴离子,在pH=3.5的酸性条件下效果最好,所以在氯化之前要将海水酸化。
(2)吹出
当海水中的Br一被氧化成Br2以后,用空气将其吹出。另外,也可以用水蒸气,使溴和水蒸气一起蒸出。
(3)吸收
目前比较多的是用二氧化硫作还原剂,使溴单质转化为HBr,再用氯气将其氧化得到溴产品。化学方程式如下: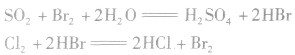
海水提镁:
(1)工艺流程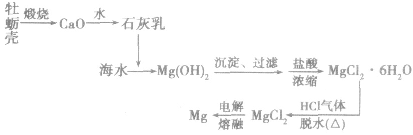
(2)主要化学反应
①制备石灰乳: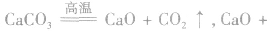
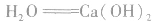
②沉淀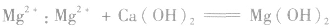
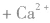
③制备
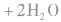
从海水中提取重水:
提取重水的方法:蒸馏法、电解法、化学交换法、吸附法等。常用方法:化学交换法(硫化氢一水双温交换法)
铀和重水目前是核能开发中的重要原料,从海水中提取铀和重水对一个国家来说具有战略意义,化学在开发海洋药物方面也将发挥越来越大的作用。潮汐能、波浪能也是越来越受到重视的新型能源。
发现相似题
与“下列过程中,涉及化学变化的是[ ]A.蒸馏法将海水淡化为饮用...”考查相似的试题有:
- 下列实验可行的是[ ]A.用澄清石灰水检验CO中含有的CO2B.用BaCl2除去NaOH溶液中混有的少量Na2SO4C.用乙醇从碘水中萃取碘D....
- 海带中含碘元素,从海带中提取碘有如下步骤:( )①通入足量Cl2②将海带焙烧成灰后加水搅拌 ③加CCl4振荡 ④用分液漏斗分液 ⑤过...
- 目前世界上60%的镁是从海水中提取的。学生就这个课题展开了讨论的。已知海水提镁的主要步骤如下学生就这个课题提出了以下问题...
- 空气吹出法工艺,是目前“海水提溴”的最主要方法之一。其工艺流程如下(1)溴在周期表中位于_______周期,_______族。(2)步...
- 以下设备名称中不属于接触法制硫酸的是A.沸腾炉B.氧化炉C.吸收塔D.接触室
- 下面是甲、乙、丙、丁四个种群,在一个达到生态平衡的环境中所含有的总能量和残留农药DDT的平均浓度。种群甲乙丙丁能量(kJ)...
- 最近,我国利用生产磷铵排放的废渣磷石膏制取硫酸并联产水泥的技术研究获得成功。具体生产流程如下:回答下列问题:(1)操作...
- 从海水中可获得的在常温下为液体的单质是[ ]A.MgB.KC.Br2D.I2
- (15分)氨基磺酸(H2NSO3H)是一元固体强酸,溶于水和液氨,不溶于乙醇,在工业上用作酸性清洗剂、阻燃剂、磺化剂等。市售商品...
- 下列过程中,涉及化学变化的是[ ]A.蒸馏法将海水淡化为饮用水B.四氯化碳萃取碘水中的碘C.过滤除去粗盐中的不溶性杂质D.三...