本试题 “(10分)草酸与高锰酸钾在酸性条件下能够发生如下反应:MnO4-+ H2C2O4+ H+— Mn2++ CO2↑+ H2O(未配平)现用4 mL 0.001 mol/L KMnO4溶液与2 mL 0.01 mol/L H2...” 主要考查您对化学反应速率的定义、公式
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 化学反应速率的定义、公式
化学反应速率:
1.定义:化学反应速率是用来衡量化学反应进行的快慢程度的物理量。
2.表示方法:在容积不变的反应器中,通常用单位时间内反应物浓度的减少或生成物浓度的增加来表示。即: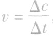
3.单位:mol·L-1·s-1或mol·L-1·min-1等。
4.注意:
(1)化学反应速率是指一段时间内的平均速率,而不是瞬时速率;通常前一段时间的平均反应速率要快于后一段时间的平均反应速率,反应速率均取正值,即v>0。
(2)在一定温度下,固体和纯液体物质单位体积的物质的量保持不变,即物质的量浓度为常数,因此在表示化学反应速率时,不代入固体或纯液体物质的浓度。浓度是指气体或溶液的浓度。
(3)同一个化学反应在相同的条件下、在同一段时间内,用不同物质表示反应速率时,数值可能相同也可能不同,但表达的意义都相同,即反应的快慢程度是一样的。
(4)在同一反应巾用不同的物质来表示反应速率时,其数值之比等于化学方程式中各物质的化学计量数之比.
如化学反应: ,
,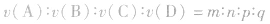 ,所以
,所以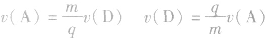
发现相似题
与“(10分)草酸与高锰酸钾在酸性条件下能够发生如下反应:MnO4...”考查相似的试题有:
- 在反应:C+CO22CO中,可使反应速率增大的措施是①增大压强 ②升高温度 ③通入CO2 ④增加碳的量 ⑤降低压强A.①②③④B.②③④⑤C.①②③D...
- 在T℃下,将1 mol N2和3 mol H2的混合气体通入固定体积为2L的密闭容器内,起始压强为101KPa,经过30s达到平衡,测得平衡混合气...
- .在容积为2 L的密闭容器中,有反应:mA(g)+nB(g)pC(g)+qD(g),经过5分钟达到平衡,此时,各物质的变化为:A减少了a...
- (14分)铅及其化合物工业生产及日常生活具有非常广泛的用途。(1)瓦纽科夫法熔炼铅,其相关反应的热化学方程式如下:2PbS(s)+3...
- 在2L的密闭容器里充入4molN2和6molH2,在一定条件下使其反应,5min后测得反应混合物中NH3占25%(体积分数),则此时用氮气表...
- 在一个密闭容器中,盛有N2和H2,它们的起始浓度分别是1.8 mol·L-1和5.4 mol·L-1,在一定的条件下它们反应生成NH3,10min后测...
- (1)(4分)某探究小组用HNO3与大理石反应过程中质量减小的方法,研究影响反应速率的因素。所用HNO3浓度为1.00mol/L、2.00mol...
- 反应2SO2+O2⇌2SO3经一段时间后,SO3的浓度增加了0.4mol•L-1,在这段时间内用O2表示的反应速率为0.04mol•L-1•s-1,则这段时间...
- 对于A2+3B22C的反应来说,以下化学反应速率的表示中,反应速率最快的是 ( )A、v(B2)=0.8 mol·L-1·s-1B、v(A2)=0.4 mol·L...
- 可逆反应:X(g)+3 Y(g)2 R(g)+2W(g)在4种不同情况下的反应速率分别如下,其中表示该反应速率最快的是( )A.v(X) = 0.15 ...