本试题 “下列有关物质性质、结构的表述均正确,且存在因果关系的是( ) 表述 I 表述II A 在水中,NaCl的溶解度比I2的溶解度大 NaCl晶体中Cl-与Na+间的离子键大于碘晶...” 主要考查您对键能、键长、键角
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 键能、键长、键角
共价键的键参数:
(1)键能:指气态基态原子形成1mol化学键释放的最低能量。键能越大,化学键越稳定。
(2)键长:指成键原子的核间距。键长越短,共价键越稳定。
注意:我们通常通过比较两原子的共价半径来比较共价单键键长的大小,但共价键的键长并不等于两原子的共价半径之和。
(3)键角:在多原子分子内,两个共价键之间的夹角。
键角是描述分子立体结构的重要参数。多原子分子的键角是一定的,表明共价键具有方向性。

说明:键长、键能决定共价键的强弱和分子的稳定性。原子半径越小,键长越短,键能越大,分子越稳定。例如, 分子中:
分子中:
X原子半径: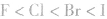
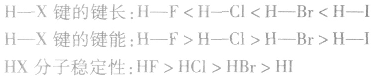
(1)键能:指气态基态原子形成1mol化学键释放的最低能量。键能越大,化学键越稳定。
(2)键长:指成键原子的核间距。键长越短,共价键越稳定。
注意:我们通常通过比较两原子的共价半径来比较共价单键键长的大小,但共价键的键长并不等于两原子的共价半径之和。
(3)键角:在多原子分子内,两个共价键之间的夹角。
键角是描述分子立体结构的重要参数。多原子分子的键角是一定的,表明共价键具有方向性。

说明:键长、键能决定共价键的强弱和分子的稳定性。原子半径越小,键长越短,键能越大,分子越稳定。例如,
 分子中:
分子中: X原子半径:
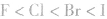
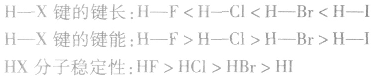
发现相似题
与“下列有关物质性质、结构的表述均正确,且存在因果关系的是( ...”考查相似的试题有:
- 已知C3N4晶体具有比金刚石更大的硬度,且原子间均以单键结合,下列关于晶体的说法正确的是( )A.C3N4晶体是分子晶体B.C3N4...
- A+、B+、C-、D、E五种粒子(分子或离子)中,每个粒子均有10个电子,已知:①A++C-==D+E↑;②B++C-==2D。请回答:(1)C-离子的电...
- 氧是地壳中含量最多的元素,下列比较中正确的是( ) A.第一电离能N>O B.稳定性:H2O>HF C.电负性:S>O D.键角:H20>...
- 已知甲烷分子中相邻两氢原子间距离为a,求其键长和键角。
- Al和Si,Ge和As在周期表处于金属元素和非金属元素的过渡区域,其单质和化合物在建筑业、电子工业和石油化工等方面应用广泛。...
- 下列有关物质性质、结构的表述均正确,且存在因果关系的是[ ]表述1 表述2 A.在水中,NaCl的溶解度比I2的溶解度大NaCl晶体中Cl...
- 下列说法中正确的是[ ]A.NH3、PCl5、BF3、NCl3分子中没有一个分子中原子的最外层电子都满足了8e-稳定结构B.P4和CH4都是正四...
- 氮化硼(BN)是一种重要的功能陶瓷材料。以天然硼砂为起始物,经过一系列反应可以得到BF3和BN,如下图所示;请回答下列问题:(1...
- (1)H+可与H2O形成H3O+,H3O+中O原子采用_______杂化,其键角比水分子_______(填“大”或“小”)。(2)下列是钠、碘、金刚石...
- 中学化学教材中提供了不少数据。下列为某同学利用相关数据作出推理和判断的依据,其中不正确的是[ ]A.依据中和热的数据,推...