本试题 “1919年,Langmui提出等电子原理:原子数相同、电子数相同的分子,互称为等电子体。等电子体的结构相似、物理性质相近。此后,等电子原理又有所发展。例如,由...” 主要考查您对杂化轨道理论(中心原子杂化方式)
等电子原理(等电子体)
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 杂化轨道理论(中心原子杂化方式)
- 等电子原理(等电子体)
杂化轨道理论:
是鲍林为了解释分子的立体结构提出的。中心原子杂化轨道、孤电子对数及与之相连的原子数间的关系是:杂化轨道数=孤电子对数+与之相连的原子数。杂化前后轨道总数比变,杂化轨道用来形成σ键或容纳孤对电子,未杂化的轨道与杂化轨道所在平面垂直,可用来形成π键。
常见杂化方式:
(1)sp杂化:直线型 如:CO2、CS2
(2)sp2杂化:平面三角形(等性杂化为平面正三角形) 如:BCl3 C2H4
不等性杂化为V字型 如:H2O H2S OF2
(3)sp3杂化:空间四面体(等性杂化为正四面体) 如:CH4、CCl4
不等性杂化为三角锥 如:NH3 PCl3 H3O+
sp3d杂化:三角双锥
sp3d2杂化:八面体(等性杂化为正八面体)
是鲍林为了解释分子的立体结构提出的。中心原子杂化轨道、孤电子对数及与之相连的原子数间的关系是:杂化轨道数=孤电子对数+与之相连的原子数。杂化前后轨道总数比变,杂化轨道用来形成σ键或容纳孤对电子,未杂化的轨道与杂化轨道所在平面垂直,可用来形成π键。
常见杂化方式:
(1)sp杂化:直线型 如:CO2、CS2
(2)sp2杂化:平面三角形(等性杂化为平面正三角形) 如:BCl3 C2H4
不等性杂化为V字型 如:H2O H2S OF2
(3)sp3杂化:空间四面体(等性杂化为正四面体) 如:CH4、CCl4
不等性杂化为三角锥 如:NH3 PCl3 H3O+
sp3d杂化:三角双锥
sp3d2杂化:八面体(等性杂化为正八面体)
分子的构型与杂化类型的关系:
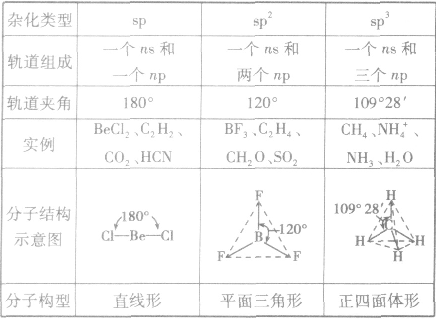
等电子原理:
1.等电子原理等电子体具有相似的化学键特征,它们的结构相似,物理性质相近,此原理称为等电子原理。例如,CO和N2的熔沸点、溶解性、分子解离能等都非常相近。
2.等电子粒子电子数相同的粒子(原子、分子、离子)称为等电子粒子。
常见的等电子粒子: 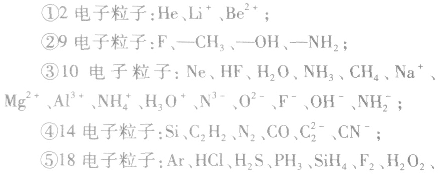
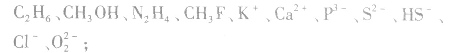
⑥核外电子总数及质子数均相等的粒子: 
3.等电子体
(1)原子总数相同、价电子总数相同的粒子互称为等电子体。如N2与CO是等电子体,但N2与C2H2不是等电子体;O2与SO2是等电子体。
(2)常见的等电子体
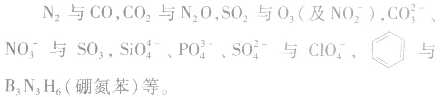
4.等电子原理的应用
(1)利用等电子原理可以较快判断一些分子或离子的构型,如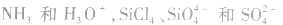 的空间构型分别是三角锥形和正四面体形。
的空间构型分别是三角锥形和正四面体形。
(2)在制造新材料方面有重要应用。如晶体硅、锗是良好的半导体材料,它们的等电子体磷化铝(AIP)、砷化镓(GaAs)也都是良好的半导体材料。,
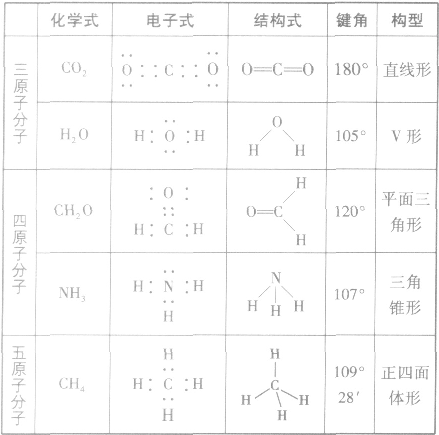
常见分子的立体结构:
发现相似题
与“1919年,Langmui提出等电子原理:原子数相同、电子数相同的分...”考查相似的试题有:
- (三选一)【化学--选修物质结构与性质】研究物质的微观结构,有助于人们理解物质变化的本质。请回答下列问题:(1)O、Si、N元...
- 有关苯分子中的化学键描述正确的是[ ]A.每个碳原子的sp2杂化轨道中的一个形成大π键B.每个碳原子的未参加杂化的2p轨道形成大...
- (1)H+可与H2O形成H3O+,H3O+中O原子采用_______杂化,其键角比水分子_______(填“大”或“小”)。(2)下列是钠、碘、金刚石...
- 下列是A、B、C、D、E五种短周期元素的某些性质ABCDE化合价-4-2-1-2-1电负性2.52.53.03.54.0(1)元素A是形成有机物的主要元素...
- 下列物质的化学用语正确的是( )A.NH4H的电子式:B.硝基苯的结构简式:C.甲烷分子的比例模型:D.sp2杂化轨道模型:
- (1)随着人们生活质量的提高,不仅室外的环境安全为人们所重视,室内的环境安全和食品安全也越来越为人们所关注.甲醛(CH2O...
- (三选一)【物质结构与性质】三氟化氮是一种无色、无味、无毒且不可燃的气体,在半导体加工、太阳能电池制造和液晶显示器制...
- (1)下表是A、B、C、D、E五种短周期元素的某些性质①A元素是形成有机物的主要元素,下列分子中采取sp和sp3两种杂化方式的是____...
- A、B、C、D、E分别代表5种粒子,每种粒子中都含有18个电子。其中A和C都是由单原子形成的阴离子,B、D和E都是由两种元素组成的...
- 下列关于等电子体的说法中,正确的是[ ]A.N2与CO不属于等电子体,故它们的熔沸点、溶解度相差较大B.PO43-与SO42-不属于等电...