本试题 “两次荣获诺贝尔奖的美国化学家鲍林,在研究含氧酸性的强弱时,提出了判断含氧酸酸性强弱的一条经验规律是:含氧酸分子结构中含非羟基氧原子数越多,该含氧酸...” 主要考查您对无机含氧酸分子的酸性
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 无机含氧酸分子的酸性
无机含氧酸:
可以的分子式为HmROn,其通式可以写成(HO)mROn,也可写成ROm-nOHn,其中R称为成酸元素,无机含氧酸在水溶液中的酸强度取决于酸分子中羟基-O-H的电离程度,也可以用Pka值来衡量。酸分子羟基中的质子在电离过程中脱离氧原子,转移到水分子中的孤对电子对上,其转移的难易程度取决于成酸元素R吸引羟基氧原子电子的能力。如果成酸无素R的电负性越大,R周围的非羟基氧原子数目越多,则其酸性越强。原因是成酸元素R的电负性越大,则其偏移O的电子越少,从而减小了O原子周围的电子密度增大的趋势,使得其对质子的吸引减弱,有利于质子的转移;非羟基氧原子越多,则分子周围越易形成离域π键,这种键将成酸R原子及O原子包裹在其中,一方面增强了羟基-O-H键的极性,有利于质子的转移,其次使得整个酸基团周围的空间减小,阻碍了质子与O原子上孤对电子的结合,从而使得酸性增强。
含氧酸的酸性一般存在如下规律:
(1)同一成酸元素若能形成几种不同氧化态的含氧酸,其酸性依氧化数递增而递增;如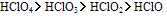
〔原因:从HClO到HClO4非羟基氧原子逐渐增多,羟基-O-H键的极性增强,质子转移程度增强,故酸性增强〕
(2)在同一主族中,处于相同氧化态的成酸元素,其含氧酸的酸性随原子序数递增,自上而下减弱。如

〔原因:同主族元素自上而下,成酸元素的电负性逐渐减小,原子半径增大,吸引羟基氧原
子的能力依次减小,羟基-O-H键的极性依次减小,所以酸性依次减弱。〕
(3)在同一周期中,处于最高氧化态的成酸元素,其含氧酸的酸性随原子序数递增,自左至右增强。如

〔原因:同一周期中,从左至右元素的非金属性逐渐增强,成酸元素的电负性逐渐增大,吸引电子对的能力逐渐减小,电子偏向成酸元素R一方的程度增大,含氧酸分子中的氢原子的极化程度增大,所以酸性增强〕
可以的分子式为HmROn,其通式可以写成(HO)mROn,也可写成ROm-nOHn,其中R称为成酸元素,无机含氧酸在水溶液中的酸强度取决于酸分子中羟基-O-H的电离程度,也可以用Pka值来衡量。酸分子羟基中的质子在电离过程中脱离氧原子,转移到水分子中的孤对电子对上,其转移的难易程度取决于成酸元素R吸引羟基氧原子电子的能力。如果成酸无素R的电负性越大,R周围的非羟基氧原子数目越多,则其酸性越强。原因是成酸元素R的电负性越大,则其偏移O的电子越少,从而减小了O原子周围的电子密度增大的趋势,使得其对质子的吸引减弱,有利于质子的转移;非羟基氧原子越多,则分子周围越易形成离域π键,这种键将成酸R原子及O原子包裹在其中,一方面增强了羟基-O-H键的极性,有利于质子的转移,其次使得整个酸基团周围的空间减小,阻碍了质子与O原子上孤对电子的结合,从而使得酸性增强。
含氧酸的酸性一般存在如下规律:
(1)同一成酸元素若能形成几种不同氧化态的含氧酸,其酸性依氧化数递增而递增;如
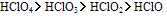
〔原因:从HClO到HClO4非羟基氧原子逐渐增多,羟基-O-H键的极性增强,质子转移程度增强,故酸性增强〕
(2)在同一主族中,处于相同氧化态的成酸元素,其含氧酸的酸性随原子序数递增,自上而下减弱。如

〔原因:同主族元素自上而下,成酸元素的电负性逐渐减小,原子半径增大,吸引羟基氧原
子的能力依次减小,羟基-O-H键的极性依次减小,所以酸性依次减弱。〕
(3)在同一周期中,处于最高氧化态的成酸元素,其含氧酸的酸性随原子序数递增,自左至右增强。如

〔原因:同一周期中,从左至右元素的非金属性逐渐增强,成酸元素的电负性逐渐增大,吸引电子对的能力逐渐减小,电子偏向成酸元素R一方的程度增大,含氧酸分子中的氢原子的极化程度增大,所以酸性增强〕
发现相似题
与“两次荣获诺贝尔奖的美国化学家鲍林,在研究含氧酸性的强弱时...”考查相似的试题有:
- 下列各组酸中,酸性依次增强的是[ ]A. H2CO3、H2SiO3、H3PO4B. HNO3、H3PO4、H2SO4C. HI、HCl、H2SD. HClO、HClO3、HClO4
- 数10亿年来,地球上的物质不断地发生变化,大气的成分也发生了很大变化。下表是原始大气和目前空气的主要成分用上表所涉及的...
- ⅥA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种氧化态,含ⅥA族元素的化合物在研究和生产中有许多重要用途。请回...
- 两次荣获诺贝尔奖的美国化学家鲍林,在研究含氧酸性的强弱时,提出了判断含氧酸酸性强弱的一条经验规律是:含氧酸分子结构中...
- 含氧酸可表示为:(HO)mROn,酸的强度与酸中的非羟基氧原子数n有关,n越大,酸性越强。一般n=0弱酸,n=1 中强酸,n=2强酸,n=3...
- 同族元素的同类物质的结构、性质既有相似性,也有特殊性。回答下列问题:(1)已知酸性FCH2COOH>CH3COOH,试推断:①BrCH2COOH、...
- 判断含氧酸强弱的一条经验规律是:含氧酸分子结构中含非羟基氧原子数越多,该含氧酸的酸性越强。如下表所示(1)亚磷酸(H3PO3)...
- 已知含氧酸可用通式(HO)nXOm来表示,如X是S,则m=2,n=2,则这个式子就表示H2SO4。一般而言,该式中m大的是强酸,m小的是弱酸...
- 下面的排序错误的是[ ]A.硬度由大到小:金刚石>碳化硅>晶体硅B.熔点由高到低:Al >Mg>NaC.晶格能由大到小: NaF> NaCl> Na...
- 下列对分子的性质的解释中,不正确的是[ ]A.水很稳定(1000℃以上才会部分分解)是因为水中含有大量的氢键所致B.乳酸()有一对...