本试题 “已知浓硫酸的密度比稀硫酸大,现将质量分数为90%和10%二种硫酸溶液等体积混合后溶质的质量分数为[ ]A.大于50%B.等于50%C.小于50%D.无法确定” 主要考查您对溶液的质量分数
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 溶液的质量分数
溶质的质量分数:
溶液质量分数= ×100%
×100%
用溶解度表示:
有关溶液的计算:

物质的量浓度与质量分数(质量百分比浓度)的比较:
| 物质的量的浓度 | 溶质的质量分数 | |
| 常用溶质的量的单位 | mol | g |
| 常用溶液的量的单位 | L | g |
| 表达式 | c(B)=n(B)/V | 溶质的质量分数= |
| 特点 | 体积相同,物质的量浓度也相同的任何溶液中,所含溶质的物质的量相同,但溶质的质量不一定相同 | 质量相同,溶质的质量分数相同的任何溶液中,所含溶质的质量相同,但溶质的物质的量不一定相同 |
物质的量浓度与质量分数之间的转化关系:
(1)基本公式: ,c为溶质的物质的量的浓度,单位mol·L-1,ρ为溶液密度,单位为g·cm-3,ω为溶质的质量分数,M为溶质的摩尔质量,单位g·mol-1。
,c为溶质的物质的量的浓度,单位mol·L-1,ρ为溶液密度,单位为g·cm-3,ω为溶质的质量分数,M为溶质的摩尔质量,单位g·mol-1。
(2)公式的推导(按溶液体积为V升推导)
 或
或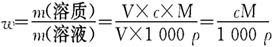
溶质的质量分数:
溶质的质量分数又叫溶液的质量百分比浓度。一般来说,(对大多数溶液)物质的量浓度越大,溶液的密度越大,质量百分比浓度也越大。但是,对于氨水、酒精溶液,物质的量浓度越大,密度越小。
溶液的混合定律:
溶质相同、质量分数分别为a%、b%的两溶液混合:
⑴等体积混合
- 当溶液的密度大于1mol/mL时,必然是溶液浓度越大,密度越大,(如硫酸、硝酸、盐酸、氢氧化钠等多数溶液)等体积混合后,质量分数
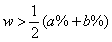 ;
; - 当溶液的密度小于1mol/mL时,必然是溶液浓度越大,密度越小,(如酒精、氨水溶液)等体积混合后,质量分数
 。
。
⑵等质量混合
两溶液等质量混合时,(无论ρ>1g/mL还是ρ<1g/mL),则混合后溶液中溶质的质量分数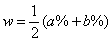
发现相似题
与“已知浓硫酸的密度比稀硫酸大,现将质量分数为90%和10%二种...”考查相似的试题有:
- 20℃时,饱和KCl溶液的密度为1.174g·cm-3,物质的量浓度为4.0mol·L-1,则下列说法中不正确的是[ ]A.25℃时,饱和KCl溶液的浓度...
- 将质量分数为5%和15%的氨水分别进行等体积混合和等质量混合,所得溶液中溶质的质量分数分别为a和b;将质量分数为5%和15%的...
- 20℃时,饱和KCl溶液的密度为1.174g/cm3,物质的量浓度为4.0mol/L,则下列说法中不正确的是[ ]A、25℃时,饱和KCl溶液的浓度大...
- 若以ω1和ω2分别表示浓度为amol·L-1和bmol·L-1氨水的质量分数,且知2a=b,则下列推断正确的是(氨水密度比水小)[ ]A.2ω1=ω2B....
- 若以ω1和ω2分别表示浓度为a mol·L-1和b mol·L-1氨水的质量分数,且知2a=b,则下列推断正确的是(氨水的密度比纯水的小)[ ]A...
- 下列说法正确的是[ ]A.所有的非金属氧化物都是酸性氧化物B.BaSO4难溶于水,是弱电解质C.福尔马林、盐酸、明矾、纯碱都是混...
- 已知浓硫酸的密度比稀硫酸大,现将质量分数为90%和10%二种硫酸溶液等体积混合后溶质的质量分数为[ ]A.大于50%B.等于50%...
- 将40℃的饱和硫酸铜溶液升温至50℃,或者温度仍保持在40℃而加入少量无水硫酸铜,在这两种情况下均保持不变的是[ ]A.硫酸铜的溶...
- 已知Ca(OH)2的溶解度随温度升高而降低。将某温度下饱和澄清石灰水①加入少量生石灰后恢复到原来温度;②降低温度。这两种情况下...
- 一定温度下,将少量生石灰放入一定量的饱和石灰水中,搅拌并冷却到原温度,下列说法正确的是[ ]A.溶质的质量增大B.溶质的物...